
【题目】已知:
2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJmol﹣1;
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJmol﹣1 .
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是( )
A.1:1
B.1:3
C.1:4
D.2:3
【答案】B
【解析】解:H2与CH4的混合气体112L,n= ![]() =5mol,设H2与CH4的物质的量分别为x、y,2H2(g)+O2(g)=2H2O(l)△H=﹣571.6kJmol﹣1 ,
=5mol,设H2与CH4的物质的量分别为x、y,2H2(g)+O2(g)=2H2O(l)△H=﹣571.6kJmol﹣1 ,
2 571.6kJ
x 285.8x
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣890kJmol﹣1 ,
1 890kJ
y 890ykJ
则 ![]() ,
,
解得x=1.25mol,y=3.75mol,
原混合气体中H2与CH4的物质的量之比是1.25mol:3.75mol=1:3,
故选B.
H2与CH4的混合气体112L,n= ![]() =5mol,设H2与CH4的物质的量分别为x、y,代入热化学反应方程式中计算热量即可解答.
=5mol,设H2与CH4的物质的量分别为x、y,代入热化学反应方程式中计算热量即可解答.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】电子工业是国民经济支柱产业之一,也是新兴科学技术发展产业.曾经电子工业常用质量分数为30%的FeCl3溶液腐蚀敷有铜箔的绝缘板,制成印刷线路板,发生反应的化学方程式为:2FeCl3+Cu═2FeCl2+CuCl2 .
(1)检验腐蚀后的溶液中是否含有Fe3+ , 应选用的试剂是 .
(2)为了从使用过的腐蚀废液中回收铜,并重新制得纯净的FeCl3溶液,采用如图所示实验步骤.请在各空格内填上适当的化学式以使实验达到预期目的.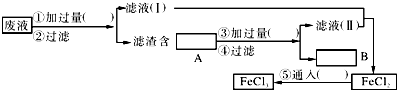
(3)写出有关化学反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将4molPCl3和2molCl2充入容积不变的密闭容器中,在一定条件下反应:PCl3+Cl2PCl5 , 各物质均为气态.达平衡后,PCl5为0.8mol.若此时再移走2molPCl3和1molCl2 , 相同温度下达到平衡,PCl5的物质的量为( )
A.0.8mol
B.0.4mol
C.0.4mol<x<0.8mol
D.<0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡是无色液体,熔点﹣33℃,沸点114℃.氯气与金属锡在加热时反应可以用来制备SnCl4 , SnCl4极易水解,在潮湿的空气中发烟.实验室可以通过图装置制备少量SnCl4 (夹持装置略). 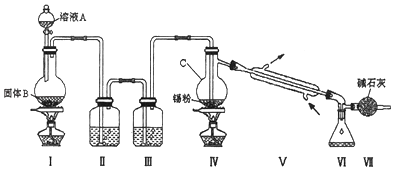
(1)仪器C的名称为:;
(2)装置Ⅰ中发生反应的离子方程式为:;
(3)装置Ⅱ中的最佳试剂为 , 装置Ⅶ的作用为;
(4)若装置连接顺序为Ⅰ﹣Ⅱ一Ⅳ一Ⅴ一Ⅵ一Ⅶ,在Ⅳ中除生成SnCl4外,还会生成的含锡的化合物的化学式为 .
(5)Ⅳ中加热的作用之一是促进氯气与锡粉反应,加热的另一作用为;
(6)若Ⅳ中用去锡粉11.9g,反应后,Ⅵ中锥形瓶里收集到23.8g SnCl4 , 则SnCl4的产率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入 10L恒容密闭容器中,发生反应X(g)+Y(g)2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=4.0×10﹣3mol/(Lmin)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用钛白工业的副产品FeSO4(含TiO2+、Al3+)可以生产电池级高纯超微细草酸亚铁.其工艺流程如图: 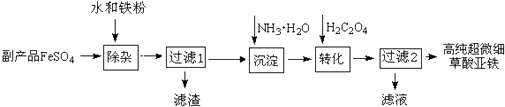
(1)已知过滤1得到的滤渣的主要成分是Al(OH)3、H2TiO3 , 请写出TiOSO4水解成 H2TiO3沉淀的化学方程式:;铁粉的作用有:①除去溶液中的Fe3+ , ② .
(2)沉淀反应的离子方程式是 .
(3)沉淀过程的反应温度为40℃,温度不宜过高的原因除控制沉淀的粒径之外,还有 .
(4)FeC2O4生成时,要在真空环境下进行,原因是 .
(5)过滤2得到的滤液经蒸发浓缩、 , 可得到副产品.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.乙醇和乙酸都存在碳氧双键
B.甲烷和乙烯都可以与氯气反应
C.酸性高锰酸钾可以氧化苯和乙醛
D.乙烯可以与氢气发生加成反应,而苯不能与氢气加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程.
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq) ![]() Na2S2O3(aq) (Ⅲ)
Na2S2O3(aq) (Ⅲ)
(1)装置A中发生的化学反应方程式为
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 .
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是 .
(4)已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是 , 装置E的作用为
(5)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O35H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂设计实验,检测产品中是否存在Na2SO4 , 简要说明实验操作,现象和结论: . 已知:Na2S2O35H2O遇酸易分解:S2O32+2H+=S↓+SO2↑+H2O供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 二氧化硅溶于水显酸性B. 二氧化硅是酸性氧化物,它不溶于任何酸
C. 二氧化硅和硅都是半导体材料D. 工业上以二氧化硅为原料生产硅
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com