
| ѡ�� | ʵ����� | ���� | ���� |
| A | �ھƾ����ϼ������� | �����ۻ��������� | �۵㣺���������� |
| B | ij���������м���Ba��OH��2��Һ | ������ɫ���� | ����������ֻ��SO42- |
| C | �ò�����պȡŨ����㵽��ɫʯ����ֽ�� | ��ֽ��� | Ũ���������ˮ�� |
| D | ʳ�üӵ��μ���ʳ��KI��Һ���ټ���CCl4������ | �²���Ϻ�ɫ | ��ʳ�üӵ��κ���KIO3 |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A������������Ӧ�����������������������۵���������۵㣬������Ĥ��ס�ۻ��������䣻
B�����ܺ�����������ӣ�
C��Ũ�����ܽ�ֽ����H��O��2��1ˮ����ʽ��ȥ��������ˮ�ԣ�
D����CCl4����Һ�ֲ㣬���Ȼ�̼���ܶȱ�ˮ����ɫ�����²㣬����Ϊ�����ṩ���Խ��ʣ�ʳ�üӵ����е����Ӻ�ʳ���е�������ӷ�Ӧ���ɵⵥ�ʣ����Կ���֤����ʳ�üӵ��κ���KIO3��
��� �⣺A������������Ӧ��������������������Ĥ��ס�ۻ��������䣬˵�����������۵���������۵㣬���Ի����ֻ�ڻ������������A����
B�����ܺ�����������ӣ������ᱵ�ǰ�ɫ��������B����
C���ò�����պȡŨ����㵽��ɫʯ����ֽ�ϣ�Ũ�����ܽ�ֽ����H��O��2��1ˮ����ʽ��ȥ��ֽ��ڣ���������ˮ�ԣ���C��ȷ��
D���ӵ���ͨ����KIO3����ʵ���CCl4���²�Ϊ�Ϻ�ɫ������Ϊ�����ṩ���Խ��ʣ�ʳ�üӵ����е����Ӻ�ʳ���е�������ӷ�Ӧ���ɵⵥ�ʣ����ɵĵ����������Ȼ�̼�����Ȼ�̼��ˮ�����ܣ���Һ�ֲ㣬���Ȼ�̼���ܶȱ�ˮ����ɫ�����²㣬����֤����ʳ�üӵ��κ���KIO3����D��ȷ��
��ѡCD��
���� ���⿼�黯ѧʵ�鷽�������ۣ��漰���������������ʡ����Ӽ����֪ʶ�����س���Ԫ�ػ��������������;�Ŀ��飬�Ƚϻ�������Ŀ�ѶȲ���


 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��̼������Һ����������������2 CO32-+SO2+H2O=2 HCO3-+SO32- | |
| B�� | ��NH4Al��SO4��2��Һ�е���Ba��OH��2��ҺʹSO42-������ȫ��2Ba2++NH4++Al3++2 SO42-+4OH-=Al��OH��3��+2BaSO4��+NH3•H2O | |
| C�� | 0.5mol/L��NaHSO3��Һ��1.0mol/L��NaClO��Һ�������ϣ�HSO3-+ClO-=SO42-+Cl-+H+ | |
| D�� | ��1 mol/L NaAlO2��Һ��1.5 mol/L HCl��Һ�����������Ȼ�ϣ�6 AlO2-+9H++3H2O=5Al��OH��3��+Al3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
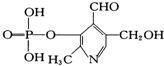 ������ȩ����ϸ������Ҫ��ɲ��֣�����Ϊ�������γɵ�������ṹʽ��ͼ�������й���������ȷ���ǣ�������
������ȩ����ϸ������Ҫ��ɲ��֣�����Ϊ�������γɵ�������ṹʽ��ͼ�������й���������ȷ���ǣ�������| A�� | �����ʵķ���ʽΪC8H9O6NP | |
| B�� | ��������������Ʒ�Ӧ���ܷ���������Ӧ������ʹʯ����Һ��� | |
| C�� | ��Ϊ�����廯��������ʿ��ܾ��з�����ζ | |
| D�� | 1mol������NaOH��Һ��Ӧ���������3mol NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
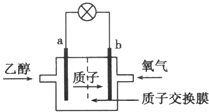 ��2004������ʥ·��˹��ѧ������һ�����͵��Ҵ���أ����û����������ܼ�����200������ʱ���磬�Ҵ���رȼ״���CH3OH�����Ч�ʸ߳�32�����Ҹ���ȫ������ܷ�ӦΪ��C2H5OH+3O2=2CO2+3H2O�����ʾ��ͼ��ͼ��ʾ������˵������ȷ���ǣ�������
��2004������ʥ·��˹��ѧ������һ�����͵��Ҵ���أ����û����������ܼ�����200������ʱ���磬�Ҵ���رȼ״���CH3OH�����Ч�ʸ߳�32�����Ҹ���ȫ������ܷ�ӦΪ��C2H5OH+3O2=2CO2+3H2O�����ʾ��ͼ��ͼ��ʾ������˵������ȷ���ǣ�������| A�� | a��Ϊ��ص����� | |
| B�� | ��ع���ʱ������b���ص��߾������ٵ�a�� | |
| C�� | ��������ĵ缫��ӦΪ��4H++O2+4e-=2H2O | |
| D�� | ��ع���ʱ��1 mol�Ҵ�������ʱ����6 mol����ת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� �� | ���ʹ��������� | ���������� | �ṹ��ʽ |
| �� | �Ҵ� | �ǻ� | CH3CH2OH |
| �� | ���� | �ǻ� | 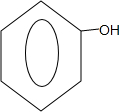 |
| ȩ | ��ȩ | ȩ�� | CH3CHO |
| ���� | ���� | �Ȼ� | CH3COOH |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com