
【题目】向200mlNaOH溶液中投入5.4gAl,二者恰好完全反应,计算:
(1)参加反应的NaOH的物质的量浓度?
(2)生成标况下氢气的体积?
【答案】
(1)解:令5.4gAl完全反应需要NaOH的物质的量为nmol,则:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
54g 2mol
5.4g nmol
所以 ![]() ;解得:n=0.2mol
;解得:n=0.2mol
所以氢氧化钠溶液的浓度为 ![]() =1mol/L;
=1mol/L;
答:参加反应的NaOH的物质的量浓度1mol/L
(2)解:令5.4gAl完全反应生成氢气的物质的量为amol,则:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
54g 3mol
5.4g amol
所以 ![]()
解得:a=0.3mol
所以生成氢气的体积为:0.3mol×22.4L/mol=6.72L
答:生成标况下氢气的体积为6.72L
【解析】(1)根据方程式计算5.4gAl完全反应需要NaOH的物质的量,再利用c= ![]() 计算氢氧化钠溶液的浓度;(2)根据方程式计算5.4gAl完全反应需要NaOH的物质的量,再根据V=nVm计算氢气的体积.
计算氢氧化钠溶液的浓度;(2)根据方程式计算5.4gAl完全反应需要NaOH的物质的量,再根据V=nVm计算氢气的体积.


科目:高中化学 来源: 题型:
【题目】关于原子核外电子排布的下列叙述不正确的是
A.核外电子总是尽可能排布在能量最低的电子层
B.每一个电子层最多可容纳的电子数为2n2
C.某原子的核外最外层最多可容纳8个电子
D.当M层为次外层时,最多可容纳18个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,以石墨为电极电解A的水溶液,并做下面一系列实验.试根据实验现象完成下列问题(电解质A的水溶液焰色反应呈紫色).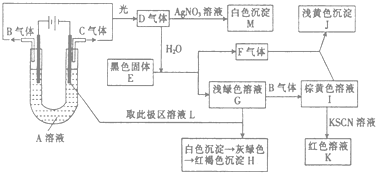
(1)A的化学式为 , E的名称为 .
(2)I和F反应的离子方程式是 .
(3)若将电解装置中的阳极换成铁棒,则在U型管底部可观察到的现象是 , 阳极的电极反应式为 , 阴极的电极反应式为 , 电解的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为苯和溴的取代反应的改进实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白:(注:溴苯与NaOH溶液通常条件下不会发生水解反应) 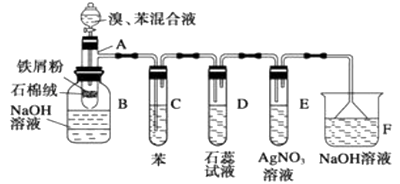
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应.写出A中所发生有机反应的化学方程式:;该反应的类型为
(2)反应开始后,观察D和E两试管,看到的现象为 D;
E;
(3)试管C中苯的作用是 .
(4)在上述整套装置中,具有防倒吸作用的仪器有(填字母): .
(5)反应2~3min后,在B中的NaOH溶液里可观察到的现象是 .
(6)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这3个优点外,还有一个优点是: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com