
| A. | 雪是由水蒸气凝华而成的,该过程有能量放出 | |
| B. | 雪融化为水后能量增加 | |
| C. | 雪融化为水时要吸收能量,导致环境温度升高 | |
| D. | 在雪上撒大量的盐(如NaCl、MgCl2等)可以融雪 |
分析 A、水蒸气凝结为雪固体,需要放热;
B、雪固体熔化为液体需要吸收能量;
C、雪固体熔化为液体需要吸收能量,环境温度降低;
D、融雪剂的主要成分是NaCl、NaNO3、CaCl2、MgCl2等盐类物质,易溶于水而电离出阴阳离子,能造成一些负面影响.
解答 解;A、雪是由水蒸气凝华而成的,气体变化为固体,该过程有能量放出,故A正确;
B、雪融化为水后,固体变化为液体过程中吸收能量,所以能量增加,故B正确;
C、雪融化为水时,固体变化为液体,吸收能量,变化过程中要吸收能量,导致环境温度降低,故C错误;
D、融雪剂的主要成分是NaCl、NaNO3、CaCl2、MgCl2等盐类物质,易溶于水而电离出阴阳离子,加速金属的锈蚀,使水质和土壤污染,故D正确;
故选C.
点评 本题考查了物质转化关系的分析判断,物质能量变化特征,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ | |
| B. | 1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ | |
| C. | 反应①的产物比反应②的产物稳定 | |
| D. | 物质的量相同时,反应②的反应物总能量比反应①的反应物总能量低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Br-<Fe2+<I- | B. | I-<Fe2+<Br- | C. | Br-<I-<Fe2+ | D. | Fe2+<Br-<I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
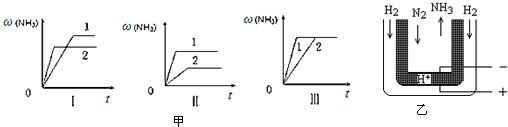
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/10-4mol.L-1 | 10.0 | 4.05 | 2.50 | 1.60 | 1.00 | 1.00 |
| c(CO)/10-3mol.L-1 | 3.60 | 3.05 | 2.85 | 2.76 | 2.70 | 2.70 |
| A. | 该反应的平衡常数和转化反应速率在夏季时比冬季时高 | |
| B. | 2~3s间的平均反应速率v(NO)=0.9 moI/(L•s) | |
| C. | 该温度下,此反应的平衡常数K=500 | |
| D. | 若该催化转化器气舱容积为2L,则达到平衡时反应放出热量0.9aJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
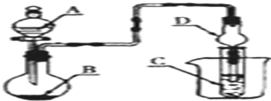
| A. | 若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色 | |
| B. | 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解 | |
| C. | 若A为醋酸,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊 | |
| D. | 若A为浓硫酸,B为Na2SO3固体,C中盛石蕊试液,则C中溶液先变红后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在lL的密闭容器中,充入1mol CO2和3mol H2,在500℃下发生反应CO2(g)+3H2(g)═CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:
在lL的密闭容器中,充入1mol CO2和3mol H2,在500℃下发生反应CO2(g)+3H2(g)═CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 消耗KMnO4溶液体积/mL | 25.00 | 25.02 | 20.00 | 24.98 |
| 实验序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 双氧水(mL) | 0.5 | 0.4 | 0.6 | 0.5 | |||
| pH | 11 | 11 | 11 | 10 | |||
| 反应时间 | 3 | 3 | 3 | 3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com