
分析 4.6g纯净的金属钠的物质的量为n(Na)=$\frac{4.6g}{23g/mol}$=0.2mol,并设Na2O,Na2O2分别为xmol,ymol则62x+78y=7①,并依据钠元素守恒则n(Na)=2n(Na2O)+
2n(Na2O2),则0.2=2x+2y②,由①②可得Na2O,Na2O2的物质的量,并根据m=nM求算质量.
解答 解:4.6g纯净的金属钠的物质的量为n(Na)=$\frac{4.6g}{23g/mol}$=0.2mol,并设Na2O,Na2O2分别为xmol,ymol则62x+78y=7①,并依据钠元素守恒则n(Na)=2n(Na2O)+2n(Na2O2),则0.2=2x+2y②,由①②可得x=0.05mol,y=0.05mol,则m(Na2O)=62g/mol×0.05mol=3.1g,m(Na2O2)=78g/mol×0.05mol=3.9g,
故答案为:3.1g;3.9g
点评 本题考查混合物的有关计算,难度不大,注意利用元素守恒确定钠元素的质量,注意对公式的理解与灵活运用.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 某固体加入稀盐酸,产生了无色气体,证明该固体一定是碳酸盐 | |
| B. | 某溶液中滴加BaCl2溶液,生成不溶于稀HNO3的白色沉淀,该溶液中一定含SO42- | |
| C. | 某无色溶液中滴入无色酚酞显红色,该溶液一定显碱性 | |
| D. | 验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加AgNO3溶液,有白色沉淀出现,证明含Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
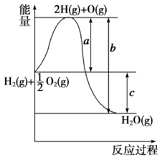 已知H2(g)+$\frac{1}{2}$O2(g)═H2O(g),反应过程中能量变化如图所示,则:
已知H2(g)+$\frac{1}{2}$O2(g)═H2O(g),反应过程中能量变化如图所示,则:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应中,每生成1mol SO42-,可脱去2mol Cl2 | |
| B. | 该反应中氧化剂是Cl2,反应消耗的氧化剂与还原剂之比为4:1 | |
| C. | 根据该反应可判断还原性:S2O32->Cl- | |
| D. | SO2也有漂白性,将SO2与氯气混合后使用,漂白性会增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag+、Cu2+、Sb3+ | B. | Cu2+、Ag+、Sb3+ | C. | Sb3+、Ag+、Cu2+ | D. | Ag+、Sb3+、Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 测定等浓度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| B | 溴乙烷与NaOH溶液共热后,加入AgNO3溶液 | 未出现淡黄色沉淀 | 溴乙烷没有水解 |
| C | 向等浓度的KCl、KI混合液中滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4, 振荡,静置 | 下层液体显紫红色 | 氧化性:Fe3+>I2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
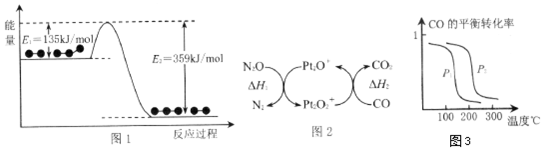
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| B. | 4.6g Na在空气中完全反应生成Na2O、Na2O2,转移0.2 NA个电子 | |
| C. | 标准状况下,将22.4L Cl2通入水中发生反应,转移的电子数为NA | |
| D. | 100g 46%的乙醇溶液中,含H-O键的数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com