
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
 溶度积/25℃ 溶度积/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:实验题
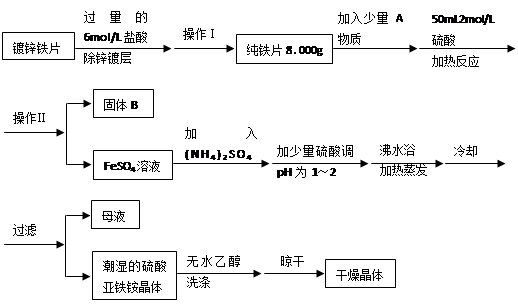
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
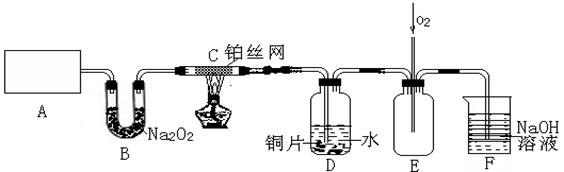 (3)D中铜片发生反应的离子方程式为___________________________,为了使Cu片溶解的速率加快,可向D处的溶液中加入下列少量物质中的___________(填下列各项序号)
(3)D中铜片发生反应的离子方程式为___________________________,为了使Cu片溶解的速率加快,可向D处的溶液中加入下列少量物质中的___________(填下列各项序号)| A.Na2CO3 | B.AgNO3 | C.H2SO4 | D.FeSO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 序号 | 实验操作 | 实验目的 |
| A | 浓、稀HNO3分别与Cu反应 | 比较浓、稀HNO3的氧化性强弱 |
| B | MgCl2、AlCl3浓液中分别通入NH3 | 比较镁、铝的金属性强弱 |
| C | 测定等浓度的Na3PO4、Na2SO4两溶液的PH | 比较磷、硫的非金属性强弱 |
| D | 用等浓度的盐酸、碳酸氢钠两溶液混合反应 | 比较盐酸、碳酸的酸性强弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
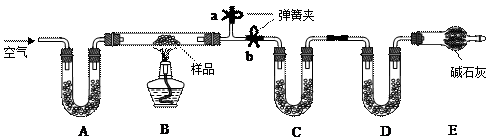
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
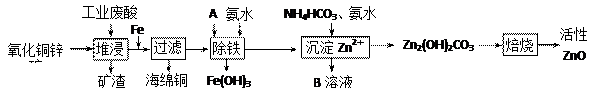
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
| A.KMnO4 | B.O2 | C.H2O2 | D.Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com