

���� ����Ԫ���������ڱ��е�λ�ÿ�֪aΪHԪ�أ�bΪAlԪ�أ�cΪCԪ�أ�dΪSiԪ�أ�eΪNԪ�أ�fΪOԪ�أ�gΪFԪ�أ�hΪClԪ�أ����Ԫ�������ɵĵݱ�����Լ���Ӧ���ʵ����ʽ��з�����
��� �⣺����Ԫ���������ڱ��е�λ�ÿ�֪aΪHԪ�أ�bΪAlԪ�أ�cΪCԪ�أ�dΪSiԪ�أ�eΪNԪ�أ�fΪOԪ�أ�gΪFԪ�أ�hΪClԪ�أ�
��1��H�ж��ֺ��أ�����һ�ֺ��غ�����һ�����ӣ��ú��ط���Ϊ12H���ʴ�Ϊ��12H��
��2�����Ӳ���Խ�࣬�뾶Խ��ͬһ���ڣ�ԭ������Խ�뾶ԽС����ԭ�Ӱ뾶��СΪ��Al��Si��C��O���ʴ�Ϊ��Al��Si��C��O��
��3��Ԫ�صķǽ�����Խǿ�����Ӧ����������ˮ���������Խǿ�����ڷǽ�����Cl��ͬ����Ԫ�ش�����Ԫ�صķǽ���������ǿ�����Ӧ������������ˮ�������������ǿ���������ԣ�HClO4��HNO3��H2CO3��H2SiO3���ʴ�Ϊ��H2SiO3��H2CO3��HNO3��HClO4��
��4�������������������Ļ�����з�����������裬Ҳ���Լ���������Һ���ٹ���ϴ�ӣ��ʴ�Ϊ��H��Cl��
���� ������Ҫ����ṹ����λ�ù�ϵ��Ԫ�������ɡ��л�����ƶ������ʡ�Ԫ�ػ��������ʵȣ��ѶȲ���ע��Ի���֪ʶ���������գ�


 �ƸԹھ��ο���ϵ�д�
�ƸԹھ��ο���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 431kJ•mol-1 | B�� | 945.6kJ•mol-1 | C�� | 649kJ•mol-1 | D�� | 896kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
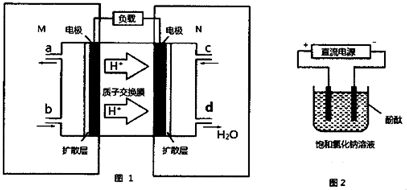
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


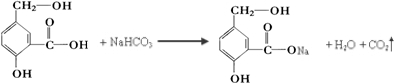
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ϡ��Ԫ���DZ����ս����Դ���ҹ����̲�����������λ��
ϡ��Ԫ���DZ����ս����Դ���ҹ����̲�����������λ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ˮ���ƾ���ˮ�����Ӻ�ˮ | |
| B�� | ���������ˮ���屽��ˮ����������ˮ | |
| C�� | ���ͺ�ˮ����ȩ��ˮ��������Ҵ� | |
| D�� | �����ˮ���ױ���ˮ������ͱ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ѹǿ | B�� | �����¶� | ||
| C�� | ����ˮ������Ũ�� | D�� | ����CO��Ũ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com