
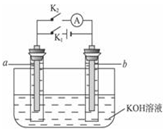
 如图所示,a、b是多孔石墨电极,某同学按图装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )
如图所示,a、b是多孔石墨电极,某同学按图装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )| A. | 断开K2,闭合K1时,a极上的电极反应式为:4OH--4e-═O2↑+2H2O | |
| B. | 断开K2,闭合K1一段时间,溶液的pH要变大 | |
| C. | 断开K1,闭合K2时,b极上的电极反应式为:2H++2e-═H2↑ | |
| D. | 断开K1,闭合K2时,OH-向b极移动 |
分析 A、断开K2,闭合K1时,形成电解池,阳极发生失电子的氧化反应;
B、断开K2,闭合K1时,相当于电解装置,根据电解氢氧化钾的工作原理来回答;
C、断开K1,闭合K2时,形成氢氧燃料电池,根据其工作原理来回答;
D、原电池中,电解质里的阴离子移向电池的负极.
解答 解:A、断开K2,闭合K1时,形成电解池,a极是阳极,氢氧根离子发生失电子的氧化反应,即4OH--4e-═O2↑十2H2O,故A正确;
B、断开K2,闭合K1时,相当于电解装置,相当于电解氢氧化钾,实质是电解水,所以氢氧化钾的浓度增大,pH要变大,故B正确;
C、断开K1,闭合K2时,形成氢氧燃料电池,在a极附近有大量的氧气,在b极附近有大量的氢气,此时b极是负极,发生失电子的氧化反应,在碱性电解质下,电极反应为:2OH-+H2-2e-═2H2O,故C错误;
D、断开K1,闭合K2时,形成氢氧燃料电池,a极是充满氧气的正极,b极是充满氢气的负极,电解质里的阴离子移向电池的负极移动,即OH-向b极移动,故D正确;
故选C.
点评 本题考查学生原电池和电解质的工作原理,是一道物理电路和化学电池联系的一道综合题目,难度较大.


科目:高中化学 来源: 题型:选择题
| A. | 从1L、1mol/L NaCl溶液中取出10mLNaCl溶液,其浓度仍为1mol/L | |
| B. | 配制0.5L、10mol/L的盐酸,需要氯化氢气体112升(标况) | |
| C. | 0.5L、2mol/L BaCl2溶液中Ba2+ 和 Cl-的总个数约为3×6.02×1023 | |
| D. | 10g、98%的浓硫酸(密度为1.84g/cm3 )与10mL、1.84mol/L的浓硫酸浓度不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 出现环境 | 实验事实 | |
| A | 以稀H2SO4为电解质的Cu-Zn原电池 | Cu为正极,正极上发生还原反应 |
| B | 电解CuCl2溶液 | 电子经过负极→阴极$\stackrel{通过电解液}{→}$阳极→正极 |
| C | 弱酸性环境下钢铁腐蚀 | 负极处产生H2,正极处吸收O2 |
| D | 将钢闸门与外加电源负极相连 | 牺牲阳极阴极保护法,可防止钢闸门腐蚀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2SO2(g)+O2(g)?2SO3(g)△H=-196kJ/mol(反应热) | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/mol(燃烧热) | |
| C. | NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| D. | 2NO2=O2+2NO△H=-116.2kJ/mol(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤ | B. | ②④ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{22.4}$mol/L | B. | $\frac{1}{36.5}$mol/L | C. | $\frac{4}{5}$×$\frac{1}{22.4}$mol/L | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生石灰 | B. | 草木灰 | C. | 明矾 | D. | 漂白粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 国庆期间燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 | |
| B. | CO、NO、NO2都是大气污染气体 | |
| C. | 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶 | |
| D. | 青铜是我国使用最早合金材料,目前世界上使用量最大合金材料是钢铁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com