
·ÖĪö ÓŠŅ»°×É«·ŪÄ©£¬æÉÄÜÓÉNaOH”¢K2SO4”¢CuSO4”¢Ba£ØOH£©2”¢CaCO3”¢BaCl2ÖŠµÄŅ»ÖÖ»ņ¼øÖÖ×é³É£¬½ųŠŠĻĀĮŠŹµŃé£ŗ
£Ø1£©Ļņ·ŪÄ©ÖŠ¼ÓČė×ćĮæĖ®£¬³ä·ÖČܽāŗó¹żĀĖ£¬µĆ°×É«³ĮµķŗĶĪŽÉ«ĀĖŅŗ£¬Ō¹ĢĢåÖŠŗ¬ÓŠ²»ČܵÄĢ¼ĖįøĘ£¬ĮķĶāBaCl2”¢Ba£ØOH£©2æÉÄÜÓėK2SO4»ņCuSO4Éś³ÉĮņĖį±µ³Įµķ£¬ĖłµĆČÜŅŗĪŖĪŽÉ«£¬ŌņŅ»¶Ø²»ŗ¬CuSO4£»
£Ø3£©£Ø2£©ÖŠ²śÉśµÄĘųĢåĪŖCO2£¬ĶØČė£Ø1£©ÖŠµÄĀĖŅŗÓÖ²śÉś°×É«³Įµķ£¬“Ė³ĮµķĪŖĢ¼Ėį±µ£¬æÉÖŖČÜŅŗĄļÓŠĒāŃõ»Æ±µ£»
£Ø4£©Č”£Ø3£©ÖŠµĆµ½µÄĀĖŅŗ¼ÓČėAgNO3ČÜŅŗŗĶĻ”ĻõĖį£¬ÓÖ²śÉś°×É«³Įµķ£¬“Ė³ĮµķĪŖĀČ»ÆŅų£®
½ā“š ½ā£ŗ£Ø1£©Ļņ·ŪÄ©ÖŠ¼ÓČė×ćĮæĖ®£¬³ä·ÖČܽāŗó¹żĀĖ£¬µĆ°×É«³Įµķ£¬øĆ³ĮµķæÉÄÜŹĒ·“Ӧɜ³ÉµÄBaSO4£¬Ņ²æÉÄÜŹĒŌ¹ĢĢåÖŠŗ¬ÓŠ²»ČܵÄĢ¼ĖįøĘ£¬Ķ¬Ź±µĆĪŽÉ«ĀĖŅŗ£¬ĖµĆ÷²»ŗ¬CuSO4£¬¹Ź“š°øĪŖ£ŗCaCO3”¢BaSO4£»CuSO4£»
£Ø2£©£Ø1£©³ĮµķæÉÄÜĪŖĢ¼ĖįøĘŗĶĮņĖį±µ£¬¼ÓČė×ćĮæŃĪĖį£¬³Įµķ²æ·ÖČܽā£¬ČܽāµÄ³ĮµķĪŖĢ¼ĖįøĘ£¬²śÉśĪŽÉ«ĘųĢåĪŖ¶žŃõ»ÆĢ¼£¬²»ČܵijĮµķĪŖĮņĖį±µ£¬æÉÖŖŌ¹ĢĢåÖŠŅ»¶ØÓŠCaCO3”¢K2SO4£¬Čܽā³ĮµķŹ±·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖCaCO3+2H+=CO2”ü+H2O+Ca2+£¬
¹Ź“š°øĪŖ£ŗCaCO3”¢K2SO4£»CaCO3+2H+=CO2”ü+H2O+Ca2+£»
£Ø3£©Ļņ£Ø1£©ÖŠµÄĀĖŅŗĶØČėCO2£¬µĆµ½Ģ¼Ėį±µ°×É«³Įµķ£¬æÉÖŖČÜŅŗĄļÓŠBa2+”¢OH-£¬
¹Ź“š°øĪŖ£ŗBa2+”¢OH-£»
£Ø4£©Č”£Ø3£©ÖŠµĆµ½µÄĀĖŅŗ¼ÓČėAgNO3ČÜŅŗŗĶĻ”ĻõĖį£¬ÓÖ²śÉśAgCl°×É«³Įµķ£¬·¢ÉśµÄĄė×Ó·“Ó¦ĪŖAg++Cl-=AgCl”ż£¬æÉÖŖČÜŅŗÖŠŗ¬ÓŠCl-£¬Ōņ¹ĢĢåÖŠŅ»¶Øŗ¬ÓŠK2SO4”¢CaCO3”¢BaCl2£¬NaOHŗĶBa£ØOH£©2ÖŠÖĮÉŁŗ¬ÓŠŅ»ÖÖ£¬
¹Ź“š°øĪŖ£ŗAg++Cl-=AgCl”ż£»K2SO4”¢CaCO3”¢BaCl2£»NaOHŗĶBa£ØOH£©2£®
µćĘĄ “ĖĢāŹĒĪļÖŹĶʶĻĢā£¬¶Ōѧɜ·ÖĪöĪŹĢā¼°½ā¾öĪŹĢāµÄÄÜĮ¦ÅąŃųÓŠŗÜ“óµÄ°ļÖś£¬ŌŚ½ā“ĖĄąĢāŹ±£¬Ź×ĻČ·ÖĪö»ģŗĻĪļÖŠø÷ĪļÖŹµÄŠŌÖŹ£¬Č»ŗó½įŗĻĢāÖŠµÄĻÖĻó·ÖĪö“ęŌŚ»ņ²»“ęŌŚµÄĪļÖŹ£¬×īŗó·µ»ŲŌĢāŃéÖ¤¼“æÉ£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ°²»ÕŹ”ø߶žÉĻµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠČČ»Æѧ·½³ĢŹ½£¬ÕżČ·µÄŹĒ£Ø £©
A£®4g¹ĢĢåĮņĶźČ«Č¼ÉÕÉś³ÉSO2£¬·Å³ö37 kJČČĮæ£ŗS(s)+O2(g)=SO2(g) ¦¤H= -296kJ/mol
B£®1molN2Óė3molH2ŌŚÄ³ĆܱÕČŻĘ÷ÖŠ·“Ó¦·Å³ö73kJČČĮ棬Ōņ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗN2(g)+3H2(g) 2NH3(g) ”÷H=-73kJ/mol
2NH3(g) ”÷H=-73kJ/mol
C£®¼×ĶéµÄ±ź×¼Č¼ÉÕČČĪŖ-890.3kJ”¤mol-1£¬Ōņ¼×ĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗCH4(g)+2O2(g)£½CO2(g)+ 2H2O(g) ”÷H=-890.3kJ”¤mol-1
D£®ĒæĖįĒæ¼īµÄÖŠŗĶČČĪŖ-57.3 kJ/mol£ŗ Ba(OH)2(aq)+H2SO4(aq)£½BaSO4(S)+2H2O(l) ”÷H=-114.6kJ/mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗž±±Ź”øßČżĮŖŗĻæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
½üÄźĄ“·¢ĻÖÓĆīę£ØCe£©µÄŃõ»ÆĪļæÉøߊ§ÖĘČ”H2£¬ÖʱøŌĄķČēĶ¼ĖłŹ¾£¬ŅŃÖŖ0£¼¦Ä£¼2£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
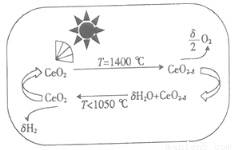
A£®Ģ«ŃōÄÜ×īÖÕ×Ŗ±äĪŖ»ÆѧÄÜ B£®CeO2ŹĒĖ®·Ö½āµÄ“߻ƼĮ
C£®T£¼1050”ꏱ£¬CeO2£¦Ä±ČCeO2ĪČ¶Ø D£®Į½²½·“Ó¦¾łŹōÓŚŃõ»Æ»¹Ō·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”øßČżÉĻµŚŅ»“ĪĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
½«Šæ”¢Ģś”¢Ķ·ŪÄ©°“Ņ»¶Ø±ČĄż»ģŗĻĶ¶Čėµ½Ņ»¶ØĮæµÄĻõĖįÖŠ£¬Ī¢ČČ£¬³ä·Ö·“Ó¦ŗó¹żĀĖ£¬ĘśČ„ĀĖŌü£¬ĀĖŅŗÖŠ ½šŹōŃōĄė×ÓĒéæö²»æÉÄÜŹĒ£Ø £©
A£®Ö»ŗ¬ Cu2 +”¢Fe2+”¢Zn2+ B£®Ö»ŗ¬ Zn2+
+”¢Fe2+”¢Zn2+ B£®Ö»ŗ¬ Zn2+
C£®Ö»ŗ¬ Fe2+”¢Zn2+ D£®Ö»ŗ¬ Cu2+”¢Fe3+”¢Zn2+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
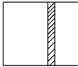 ŗćĪĀĻĀ£¬a mol AŗĶb mol BŌŚČēĶ¼ĖłŹ¾»īČūæÉ×ŌÓÉ»¬¶ÆµÄČŻĘ÷ÖŠ·¢ÉśČēĻĀ·“Ó¦£ŗA£Øg£©+2B£Øg£©?2C£Øg£©£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā£¬Éś³Én mol C£®ŌņĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©
ŗćĪĀĻĀ£¬a mol AŗĶb mol BŌŚČēĶ¼ĖłŹ¾»īČūæÉ×ŌÓÉ»¬¶ÆµÄČŻĘ÷ÖŠ·¢ÉśČēĻĀ·“Ó¦£ŗA£Øg£©+2B£Øg£©?2C£Øg£©£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā£¬Éś³Én mol C£®ŌņĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | ĪļÖŹA”¢BµÄ×Ŗ»ÆĀŹÖ®±ČĪŖa£ŗb | |
| B£® | ĘšŹ¼Ź±æĢŗĶ“ļĘ½ŗāŗóČŻĘ÷ÖŠµÄŃ¹Ēæ±ČĪŖ£Øa+b£©£ŗ£Øa+b-$\frac{n}{2}$£© | |
| C£® | ČōĘšŹ¼Ź±·ÅČė2a mol AŗĶ2b mol B£¬Ōņ“ļĘ½ŗāŹ±Éś³É2n mol C | |
| D£® | µ±vÕż£ØA£©=2vÄę£ØB£©Ź±£¬æÉÅŠ¶Ø·“Ó¦“ļµ½Ę½ŗā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  µĪ¼ÓŅŗĢåŅ©Ę· | B£® |  ¹żĀĖ | C£® |  Ļ”ŹĶÅØĮņĖį | D£® |  ¶ĮČ”ŅŗĢåµÄĢå»ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė®½āĘ½ŗāÕżĻņŅĘ¶Æ | B£® | ø÷Ī¢Į£ÅØ¶Č¾ł±äŠ” | ||
| C£® | ČÜŅŗÖŠĄė×ÓŹżÄæŌö¶ą | D£® | c£ØAl3+£©Óėc£ØSO42-£©µÄ±ČÖµ¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2OČÜÓŚĖ®£ŗNa2O+H2O=2Na++2OH- | |
| B£® | ĻņCa£ØClO£©2ČÜŅŗÖŠĶØČė¹żĮæCO2£ŗ2ClO-+H2O+CO2=2HClO+CO32- | |
| C£® | ÓĆFeCl3ČÜŅŗøÆŹ“Ķ°å£ŗFe3++Cu=Fe2++Cu2+ | |
| D£® | Ģ¼ĖįøĘČÜÓŚĻ”“×Ėį£ŗCaCO3+2H+=Ca2++CO2”ü+H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com