
| A. | CaCl2 | B. | KOH | C. | NH3•H2O | D. | H2SO4 |
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,17g甲基(-14CH3)所含的中子数为8NA | |
| B. | 0.1molFe与0.1molCl2充分反应,转移的电子数为0.2NA | |
| C. | 标准状况下,44.8LNO与22.4LO2混合后气体的分子总数为2NA | |
| D. | 1molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题




| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某有机物燃烧只生成CO2和H2O,且二者的物质的量相等,则此有机物的组成为CnH2n | |
| B. | 相同质量的烃,完全燃烧时,含氢元素质量分数越高的烃,消耗O2量越多 | |
| C. | 常温下分子中氢原子数为4的气态烃,与足量O2完全燃烧时,反应前后气体总体积不变 | |
| D. | 烃在足量的氧气中燃烧并通过浓H2SO4,减少的体积就是生成的水蒸气的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量之比 | B. | 体积比 | C. | 碳、氧原子个数比 | D. | 氢、氧原子个数比 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某沿海城市技术开发公司研制的海水淡化膜--资源问题 | |
| B. | 用石灰法进行工业废气脱硫--污染问题 | |
| C. | 研制用纯净的二氧化硅做光导纤维--能源问题 | |
| D. | 中科院研制的新型钛合金用于航空航天--材料问题 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠溶液中滴入氢氧化钙溶液:HCO3-+OH-=CO32-+H2O | |
| B. | 氢氟酸腐蚀玻璃:SiO2+4HF=SiF4↑+2H2O | |
| C. | 硫化钡加入稀硫酸:BaS+2H+=H2S↑+Ba2+ | |
| D. | 铝与氢氧化钠溶液反应:Al+2OH-=AlO2-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
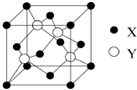 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层的3倍;元素W基态原子的核外电子共有16种运动状态.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层的3倍;元素W基态原子的核外电子共有16种运动状态.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com