
| A. | 20% | B. | 略大于20% | C. | 略小于20% | D. | 80% |
分析 硼元素的相对原子质量是10.8,则硼元素的摩尔质量是10.8g/mol,再根据$\overline{M}$=$\frac{m}{n}$计算其物质的量之比,利用物质的量计算11B物质的量分数.
解答 解:硼元素的相对原子质量是10.8,则硼元素的摩尔质量是10.8g/mol,
设10B和11B的物质的量分别是xmol、ymol,则$\frac{10g/mol×xmol+11g/mol×ymol}{(x+y)mol}$=10.8g/mol,
解得x:y=1:4,设10B和11B的物质的量分别是1mol、4mol,
则对115B的物质的量分数是$\frac{4mol}{1mol+4mol}$×100%=80%,
故选D.
点评 本题考查物质的量的计算,为高频考点,把握元素的平均摩尔质量及物质的量比等于原子个数比为解答的关键,侧重分析与计算能力的考查,题目难度不大.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 利用海水制取氯化钠、烧碱、纯碱、氯气等物质都发生了氧化还原反应 | |
| B. | 蛋白质、葡萄糖、纤维素、油脂等都能在人体内水解并提供能量 | |
| C. | 为了提高生活用水的卫生标准,自来水厂常使用Cl2和CuSO3•5H2O进行消毒、净化、以改善水质 | |
| D. | 塑料、合成橡胶和纤维这三大合成材料,都主要以石油、煤和天然气为原料生产的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅胶多孔,吸水能力强,是最好的食品干燥剂 | |
| B. | 硅的化学性质不活泼,常温下不与任何物质起反应 | |
| C. | 硅的导电性能介于导体和绝缘体之间,是良好的半导体材料 | |
| D. | Na2SiO3溶液俗称水玻璃,可用作木材防火剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
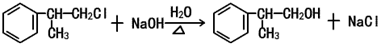
 (X为卤素原子)
(X为卤素原子)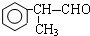 的物质,该物质是一种香料.
的物质,该物质是一种香料.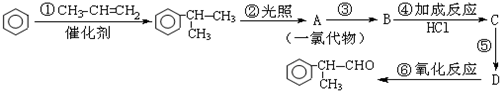
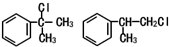 .
.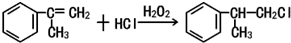 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在两支试管中分别加入3mL稀盐酸(均足量),将两个各装有0.3g NaHCO3和Na2CO3粉末的小气球分别套在两支试管口上.将气球内的NaHCO3和Na2CO3同时倒入试管中.
在两支试管中分别加入3mL稀盐酸(均足量),将两个各装有0.3g NaHCO3和Na2CO3粉末的小气球分别套在两支试管口上.将气球内的NaHCO3和Na2CO3同时倒入试管中.| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后最高或最低温度 |
| ① | 50mL水 | 2.5gNaHCO3固体 | 20℃ | 18.5℃ |
| ② | 35mL水 | 3.2gNa2CO3固体 | 20℃ | 23.3℃ |
| ③ | 35mL稀盐酸 | 含2.5gNaHCO3的 饱和溶液15mL | 20℃ | 18.8℃ |
| ④ | 50mL稀盐酸 | 含3.2gNa2CO3的 饱和溶液15mL | 20℃ | 21.2℃ |
| ⑤ | 50mL稀盐酸 | 2.5gNaHCO3固体 | 20℃ | 17.4℃ |
| ⑥ | 50mL稀盐酸 | 3.2gNa2CO3固体 | 20℃ | 24.4℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
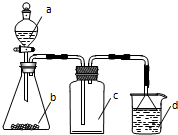 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质能完成相关实验的是( )
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质能完成相关实验的是( )| 选项 | a中物质 | b中物质 | c中的气体 | d中物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 稀硝酸 | Cu | NO | H2O |
| C | 硫酸 | Na2CO3 | CO2 | NaOH溶液 |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
| A | Fe2+、NO3-、K+ | 稀H2SO4 | 3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
| B | Fe3+、I-、ClO- | NaOH溶液 | Fe3++3OH-═Fe(OH)3↓ |
| C | Mg2+、HCO3-、Cl- | NaOH溶液 | HCO3-+OH-═CO32-+H2O |
| D | Al3+、Cl-、NO3- | 稀氨水 | Al3++3OH-═Al(OH)3↓ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com