
【题目】短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素。试回答下列问题:
(1)A在周期表中的位置是____________________, D的离子结构示意图____________。
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是________________。(用离子符号回答)
(3)写出B在空气中燃烧产物的电子式_________,该产物所含有的化学键类型有___________。
(4)在实验室里,D的单质常用B的最高价氧化物的水化物溶液来吸收,写出该反应的离子方程式_______________________________________________________________ 。
【答案】 第二周期第VIA族 ![]() S2->O2- >Na+
S2->O2- >Na+ ![]() 离子键、非极性键 Cl2 + 2OH- =Cl- + ClO- + H2O
离子键、非极性键 Cl2 + 2OH- =Cl- + ClO- + H2O
【解析】A原子的最外层电子数是次外层电子数的3倍,则A为O元素;B是短周期元素中原子半径最大的主族元素,则B为Na元素.短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,则C为S元素;B、C、D同周期,则D为Cl元素。即A为O元素;B为Na元素;C为S元素;D为Cl元素。(1)A为O氧元素,在周期表中的位置是第二周期第VIA族;D为Cl元素,核内质子数为17,有3个电子层,最外层电子数为7,原子结构示意图![]() ;(2)A、B、C元素形成的简单离子分别是O2-、Na+、S2-,Na+、O2-离子的核外电子排布相同,核电荷数越大,离子半径越小,所以离子半径O2->Na+,S2->O2-的最外层电子数相同,电子层越多,离子半径越大,所以离子半径S2->O2-,所以离子半径S2->O2->Na+;(3)钠在空气中燃烧产物是Na2O2,其电子式为:
;(2)A、B、C元素形成的简单离子分别是O2-、Na+、S2-,Na+、O2-离子的核外电子排布相同,核电荷数越大,离子半径越小,所以离子半径O2->Na+,S2->O2-的最外层电子数相同,电子层越多,离子半径越大,所以离子半径S2->O2-,所以离子半径S2->O2->Na+;(3)钠在空气中燃烧产物是Na2O2,其电子式为:![]() ;该产物所含有的化学键类型有离子键、非极性键;(4)在实验室里,氯气常用氢氧化钠溶液来吸收,反应离子方程式为Cl2 + 2OH- =Cl- + ClO- + H2O。
;该产物所含有的化学键类型有离子键、非极性键;(4)在实验室里,氯气常用氢氧化钠溶液来吸收,反应离子方程式为Cl2 + 2OH- =Cl- + ClO- + H2O。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】不用其他试剂鉴别:①NaOH ②KCl ③Mg(NO3)2 ④CuSO4四种溶液,先直接鉴别出一种,再逐一鉴别其余物质,则正确的鉴别顺序是( )
A. ④①③② B. ①④③② C. ①③④② D. ④②①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢是一种液体,易分解为水和氧气,常作氧化剂、漂白剂和消毒剂,为贮存、运输、使用的方便,工业常将H2O2转化为固态的过碳酸钠晶体(其化学式为2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠晶体失效的是
A.MnO2 B.H2S C.稀盐酸 D.NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①—⑩在表中的位置回答下列问题。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(1)③和⑧的最高价含氧酸的酸性强弱关系是_____________________________(用化学式填写)。
(2)⑥、⑦、⑩的简单离子的离子半径由大到小的顺序是________________(用离子符号表示)。
(3)由⑨与⑩形成的某种分子中各原子都满足最外层为8电子结构,其化学式是_________;由⑤与⑥形成的某种化合物中含有两类化学键,该化合物的电子式为___________。
(4)⑦的最高价氧化物对应水化物与⑥的最高价氧化物对应水化物反应的离子方程式为:________。
(5)⑧与⑩相比,非金属性较强的是_______(用元素符号表示),下列事实能证明这一结论的是_______(填字母序号)
a. 常温下⑧的单质呈固态,⑩的单质呈气态
b. ①与⑧和⑩形成的化合物分别为X和Y,稳定性Y>X
c. ⑧与⑩形成的化合物中⑧呈正价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫酸铝溶液为原料之一,在实验室里制取少量Al(OH)3,并且易于分离,最好向溶液中加入( )
A. 氢氧化钠溶液 B. 氢氧化钡溶液
C. 氨水溶液 D. 澄清的石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三种一元酸HA、HB、HC的钠盐分别为NaA、NaB、NaC,它们的物质的量浓度相同时,溶液的PH依次为9,10,8.则这三种弱酸的酸性由强到弱的顺序是( )
A. HA>HB>HC B. HB>HA>HC C. HC>HB>HA D. HC>HA>HB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于合金性质的说法中,错误的是( )
A. 合金的硬度一般比其各成分金属的硬度高
B. 合金的熔点一般比其各成分金属的熔点低
C. 合金的物理性质一般与其各成分金属的的物理性质不同
D. 合金的化学性质一般与其各成分金属的的化学性质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】E、F、D、X、Y、Z为前四周期元素,且原子序数依次增大。E的最高正价和最低负价的绝对值相等,F有三个能级,且每个能级上的电子数相等,D原子未成对电子数在同周期元素中最多,X与D同周期,第一电离能比D低,Y与F同主族,Z的最外层只有一个电子,其它电子层电子均处于饱和状态。请回答下列问题:
(1)Y原子基态核外电子排布式为__________;基态Z原子中电子占据的最高能层符号为_________。
(2)F、D、X的电负性由小到大的顺序为__________(用元素符号表示)。
(3)E、F、D、X形成的有机物FX(DE2)2中F的杂化轨道类型为____________,DX3-离子的立体构型是___________。
(4)下列关于F2E2分子和E2X2分子的说法正确的是________。
a.分子中都含σ键和π键 b.F2E2分子的沸点明显低于E2X2分子
c.都是含极性键和非极性键的非极性分子 d.互为等电子体
(5)将Z单质的粉末加入到DE3的浓溶液中,并通入X2,充分反应后溶液呈深蓝色,该反应的离子方程式为________。
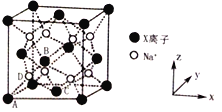
(6)X和Na的一种离子化合物的晶胞结构如图,该离子化合物为_________(填化学式)。Na+的配位数为_________。晶胞有两种基本要素,一种是原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0, ![]() ),C为(
),C为(![]() ,
, ![]() ,0),则D原子的坐标参数为________。另外一种是晶胞参数,如已知该晶胞的密度为ρg cm-3,阿伏加德罗常数为NA,则两个最近的X离子间距离为________nm(用含ρ、NA的计算式表示)。
,0),则D原子的坐标参数为________。另外一种是晶胞参数,如已知该晶胞的密度为ρg cm-3,阿伏加德罗常数为NA,则两个最近的X离子间距离为________nm(用含ρ、NA的计算式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、写出下列化合物的名称或结构简式:
①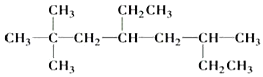 的名称为________________________.
的名称为________________________.
②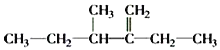 的名称为______________________________.
的名称为______________________________.
II、已知有机化合物X中各元素的质量分数分别为C---60%,H---13.3%,O---26.7%。
请填空:
(1)有机物X的实验式为____________。若0.1molX在足量氧气中充分燃烧需消耗氧气10.08L(标准状况),则X的分子式为________。
(2)实验表明:X能与金属钠反应产生H2。X分子的核磁共振氢谱中有4个吸收峰,且面积之比为3:2:2:1,则X分子中含有的官能团的名称为_________,X的结构简式为_____________。
(3)X有两种同分异构体Y和Z,其中Y能与金属钠反应产生H2,而Z不能。则Y、Z的结构简式分别为_______________、_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com