
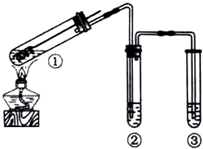
| A. | 为确认CuSO4生成,向①中加水,观察颜色 | |
| B. | 上下移动①中铜丝可控制SO2的量 | |
| C. | ②中选用品红溶液验证SO2的生成 | |
| D. | ③中选用NaOH溶液吸收多余的SO2 |
分析 A.Cu和浓硫酸在加热条件下反应生成硫酸铜,硫酸铜溶液呈蓝色;
B.在加热条件下,Cu丝和浓硫酸接触才能发生反应;
C.二氧化硫能使品红溶液褪色;
D.二氧化硫属于酸性氧化物,能和碱反应生成盐和水.
解答 解:A.Cu和浓硫酸在加热条件下反应生成硫酸铜,硫酸铜溶液呈蓝色,所以不需要向①中加水检验硫酸铜,故A错误;
B.在加热条件下,Cu丝和浓硫酸接触才能发生反应,所以上下移动①中铜丝可控制SO2的量,故B正确;
C.二氧化硫能和有色物质反应生成无色物质而具有漂白性,二氧化硫能使品红溶液褪色,则可以用品红溶液检验二氧化硫,故C正确;
D.二氧化硫有毒,不能直接排空,但二氧化硫属于酸性氧化物,能和碱反应生成盐和水,所以可以用NaOH溶液处理尾气,故D正确;
故选A.
点评 本题以浓硫酸和铜的反应为载体考查浓硫酸性质,侧重考查元素化合物知识及基本操作,知道二氧化硫具有漂白性、还原性、氧化性且属于酸性氧化物,注意从性质及环保方面分析解答,题目难度不大.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:解答题
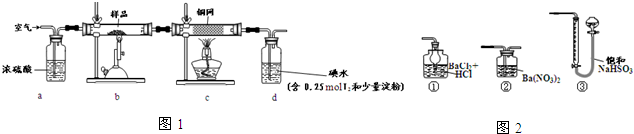
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ⑥⑦ | C. | ④⑥⑦ | D. | ⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2使溴水褪色,显示了SO2的漂白性 | |
| B. | SO2使溴水褪色,显示了SO2的还原性 | |
| C. | 从溴水中提取单质溴,可以用乙醇进行萃取 | |
| D. | SO2使溴水褪色和使品红褪色原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、K+、Cl-、NO3- | B. | K+、A13+、Cl-、AlO2- | ||
| C. | Na+、K+、CO32-、NO3- | D. | A13+、Cu2+、SO42-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
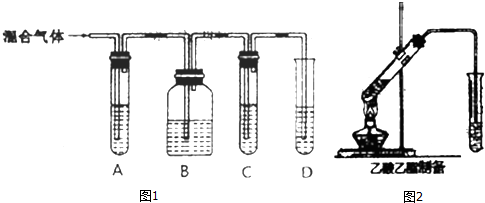
 CH3COOCH2CH3+H2O,该反应类型为酯化反应(取代反应).
CH3COOCH2CH3+H2O,该反应类型为酯化反应(取代反应).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com