
在一密闭烧瓶中,在25℃时存在着平衡:2NO2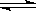 N2O4(正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是
N2O4(正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是
①颜色 ②平均分子量 ③质量 ④压强 ⑤密度
A.①和③ B.②和④ C.④和⑤ D.③和⑤
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列反应中,属于氧化还原反应的是 ( )
A、 CaCO3+2HCl === CaCl2+CO2↑+H2O B、Cu(OH)2 CuO+H2O
CuO+H2O
C 、Fe2O3+6HCl === 2 FeCl3+3H2O D、NH4NO3  N2O↑+2H2O
N2O↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
将固体A置于密闭容器中,在一定温度下发生下列反应:
①A(s)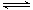 B(g)+C(g);②2C(g)
B(g)+C(g);②2C(g)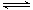 D(g)+E(g)。
D(g)+E(g)。
达到平衡时,c(D)=0.5mol·L-1,c(C)=4mol·L-1,则此温度下反应①的平衡常数为 ( )
A.25 B.20 C.16 D.9
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨反应的平衡状态是指下列情况中的
A.氢气的消耗速率与氨生成的速率之比为3︰2
B.体积不变时,混合气体的密度不再改变
C.氮气的生成速率与氨的生成速率之比为1︰2
D.容器内物质的总质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应2SO2(g)+O2(g)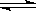 2SO3(g)从正方向开始,并达到了平衡,此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是:
2SO3(g)从正方向开始,并达到了平衡,此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是:
A.新平衡体系中,SO2和O2物质的量之比仍为2∶1
B.平衡向正反应方向移动,原因是正反应速率增大,逆反应速率减小
C.新平衡体系与旧平衡体系比较,SO3的浓度肯定增大
D.若所采取的措施是缩小容器的容积,则新旧平衡中SO2和O2的转化率之比都是1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,甲、乙两杯醋酸稀溶液,甲的pH=a,乙的pH=a+1,对下列叙述的判断正确的是
A.甲中水电离出来的H+的物质的量浓度是乙中水电离出来的H+的物质的量浓度的10倍
B.物质的量浓度c(甲)>10c(乙)
C.中和等物质的量的NaOH溶液需甲、乙两杯醋酸溶液的体积,V(甲)=10V(乙)
D.甲中的c(OH-)为乙中的c(OH-)的10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
0.1 mol/L CH3COOH溶液中存在如下电离平衡:CH3COOH  CH3COO-+H+。
CH3COO-+H+。
对于该平衡,下列叙述正确的是
A.加入水时,溶液中c(H+) 和c(OH—) 都减小
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1mol/L HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、M、Z四种短周期主族元素的原子半径依次减小,X、Y、Z的电子层数之和为5,X元素原子的最外层电子数是它的电子层数的2倍,Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,M是地壳中含量最多的元素。下列说法不正确的是( )
A.化合物YZ3极易溶解于水
B.Z与M可以形成共价化合物
C.12 g 14X中含有质子的物质的量为6 mol
D.由上述四种元素组成的离子化合物受热易分解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com