
【题目】有关化学键的说法正确的是( )
A.全部由非金属元素构成的化合物一定是共价化合物
B.某元素的原子最外层只有一个电子,它跟卤素结合时,所形成的化学键一定是离子键
C.金属与非金属原子间只能形成离子键
D.含有共价键的化合物不一定是共价化合物
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是 ( )


A. 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B. 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C. 在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D. 该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 乙醇和汽油(从石油中提炼)都是可再生能源,应大力推广“乙醇汽油”
B. 推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应
C. 氢能具有的优点是原料来源广、热值高、储存方便、制备工艺廉价易行
D. 氢能是一次能源(从自然界中以现成形式提供的能源为一次能源)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于sp3杂化轨道说法正确的是( )
A. 凡是中心原子采取sp3杂化方式成键的分子其几何构型都是四面体
B. ![]() 分子中的
分子中的![]() 杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的
杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的
C. 金刚石是三维网状结构,由碳原子从sp3杂化轨道形成共价键
D. NH3和BF3分子中,中心原子均采用sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验制备供氧剂氢化钙(CaH2),实验装置如下图所示。
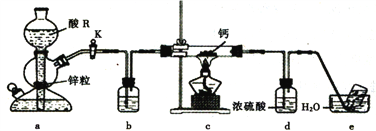
已知:①钙能与H2O、HCl、O2等反应;②氢化钙遇水剧烈反应。下列说法正确的是
A. 相同条件下,粗锌(含少量铜)比纯锌反应速率慢
B. 酸R为浓盐酸,装置b中盛装浓硫酸
C. 实验时先点燃酒精灯,后打开活塞K
D. 装置d的作用是防止水蒸气进入硬质玻璃管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有以下反应方程式:
A.CuO+H2![]() Cu+H2O
Cu+H2O
B.2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
C.Cl2+2NaOH==NaCl+NaClO+H2O
D.2FeBr2+3Cl2=2FeCl3+2Br2
E.MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
F.KClO3+6HCl(浓)=KC1+3H2O+3Cl2↑
G.HgS+O2=Hg+SO2
I.按要求将上述化学方程式序号填入相应空格内:
(1)一种单质使一种化合物中的一种元素被还原____________________;
(2)同一种物质中,同种元素间发生氧化还原反应________________;
(3)所有元素均参加氧化还原反应的是____________________________。
II.已知方程式F:KClO3+6HCI(浓)=KCl+3H2O+3Cl2↑。
(1)请用双线桥法标出电子转移的方向和数目_______________________;
(2)标准状况下当有33.6L的氯气放出时,转移电子的数目是_________________________;
(3)上述反应中氧化产物和还原产物的质量比为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H+(aq)+OH﹣(aq)═H2O(l);△H1;②2SO2(g)+O2(g)2SO3(g);△H2 . 其他条件不变时,改变反应物的量,则下列判断正确的是( )
A.△H1 , △H2都不变
B.△H1 , △H2都增大
C.△H1 , △H2都减小
D.不能确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com