
 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$ +2H2O;②E→M:2HOCH2CH2COOH$→_{△}^{浓H_{2}SO_{4}}$
+2H2O;②E→M:2HOCH2CH2COOH$→_{△}^{浓H_{2}SO_{4}}$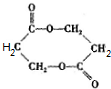 +2H2O;
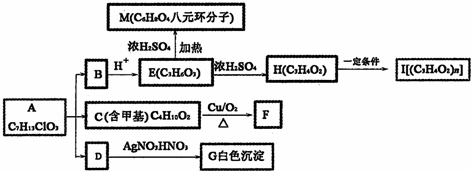
+2H2O;分析 A在NaOH溶液中水解生成B、C和D,发生了酯的水解和卤代烃的水解,B酸化得到E,故E中含有羧基,E转化为H,H在一定条件下反应生成I,反应前后各元素的组成比不变,说明H转化I应为加聚反应,则H中含有C=C,则H为CH2=CHCOOH,I为 ,E发生酯化反应成八元环状化合物生成M,可知E为HOCH2CH2COOH,M为
,E发生酯化反应成八元环状化合物生成M,可知E为HOCH2CH2COOH,M为 ,B为HOCH2CH2COONa,A在碱性条件下生成HOCH2CH2COONa、NaCl和C,D与硝酸银、硝酸反应得到白色沉淀G,故D为NaCl,G为AgCl.C的分子式为C4H10O2,分子中含有甲基,由C催化氧化生成F(C4H6O2),1molF与足量的新制银氨溶液水浴加热充分反应可生成4molAg,则F分子中含有2个-CHO,故C为
,B为HOCH2CH2COONa,A在碱性条件下生成HOCH2CH2COONa、NaCl和C,D与硝酸银、硝酸反应得到白色沉淀G,故D为NaCl,G为AgCl.C的分子式为C4H10O2,分子中含有甲基,由C催化氧化生成F(C4H6O2),1molF与足量的新制银氨溶液水浴加热充分反应可生成4molAg,则F分子中含有2个-CHO,故C为 ,F为
,F为 ,所以有机物A为
,所以有机物A为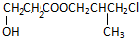 或
或 ,据此解答.
,据此解答.
解答 解:A在NaOH溶液中水解生成B、C和D,发生了酯的水解和卤代烃的水解,B酸化得到E,故E中含有羧基,E转化为H,H在一定条件下反应生成I,反应前后各元素的组成比不变,说明H转化I应为加聚反应,则H中含有C=C,则H为CH2=CHCOOH,I为 ,E发生酯化反应成八元环状化合物生成M,可知E为HOCH2CH2COOH,M为
,E发生酯化反应成八元环状化合物生成M,可知E为HOCH2CH2COOH,M为 ,B为HOCH2CH2COONa,A在碱性条件下生成HOCH2CH2COONa、NaCl和C,D与硝酸银、硝酸反应得到白色沉淀G,故D为NaCl,G为AgCl.C的分子式为C4H10O2,分子中含有甲基,由C催化氧化生成F(C4H6O2),1molF与足量的新制银氨溶液水浴加热充分反应可生成4molAg,则F分子中含有2个-CHO,故C为
,B为HOCH2CH2COONa,A在碱性条件下生成HOCH2CH2COONa、NaCl和C,D与硝酸银、硝酸反应得到白色沉淀G,故D为NaCl,G为AgCl.C的分子式为C4H10O2,分子中含有甲基,由C催化氧化生成F(C4H6O2),1molF与足量的新制银氨溶液水浴加热充分反应可生成4molAg,则F分子中含有2个-CHO,故C为 ,F为
,F为 ,所以有机物A为
,所以有机物A为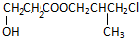 或
或 ,
,
(1)由上述分析可知,A为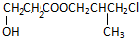 或
或 ,含有官能团为:酯基-COOC-、羟基-OH、氯原子-Cl,
,含有官能团为:酯基-COOC-、羟基-OH、氯原子-Cl,
故答案为:酯基;羟基;
(2)根据上面的分析可知,E→M为酯化反应或取代反应,C→F为氧化反应,故答案为:酯化反应或取代反应;氧化反应;
(3)①C→F的反应方程式为: +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$ +2H2O,
+2H2O,
②E→M的反应方程式为:2HOCH2CH2COOH$→_{△}^{浓H_{2}SO_{4}}$ +2H2O,
+2H2O,
故答案为: +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$ +2H2O;2HOCH2CH2COOH$→_{△}^{浓H_{2}SO_{4}}$
+2H2O;2HOCH2CH2COOH$→_{△}^{浓H_{2}SO_{4}}$ +2H2O;
+2H2O;
(4)有机物J满足下列条件:①J为E的同系物的同分异构体,且比E多两个碳原子,E为HOCH2CH2COOH,则J中有5个碳原子、三个氧原子,10个氢原子;②J能够发生银镜反应,则J中有醛基;③J水解产物不存在两个羟基连在同一个碳上,说明J能水解,即有酯基;则J的同分异构体有 HCOOCH2C(CH3)2OH、HCOOCH2CH2CH2CH2OH、HCOOCH2CH2CHOHCH3、HCOOCH2CHOHCH2CH3、HCOOCH2CH(CH3)CH2OH、HCOOCH(CH3)CH2CH2OH、HCOOCH(CH3)CHOHCH3、HCOOCH(CH2OH)CH2CH3、HCOOC(CH3)2CH2OH,共9种;其中核磁共振氢谱只有四组峰的是 HCOOCH2C(CH3)2OH、HCOOC(CH3)2CH2OH,
故答案为:9;HCOOCH2C(CH3)2OH、HCOOC(CH3)2CH2OH.
点评 本题考查有机物的推断、官能团、有机反应类型等,注意结合有机物的分子式进行推断,需要学生熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:解答题
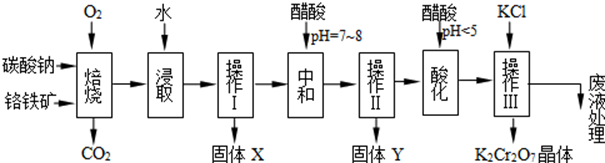
| 物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度(g/100g水) | 0℃ | 28 | 35.7 | 4.7 | 163 |
| 40℃ | 40.1 | 36.4 | 26.3 | 215 | |
| 80℃ | 51.3 | 38 | 73 | 376 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -69.4kJ•mol-1 | B. | -45.2kJ•mol-1 | C. | +69.4kJ•mol-1 | D. | +45.2kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | |||
| Y | Z |
| A. | X和Y都是非金属元素,其中X最高化合价为+5 | |
| B. | X、W的最高价氧化物在一定条件下能反应 | |
| C. | 元素X、W和氧元素可形成化学式为W2XO3,离子化合物 | |
| D. | Y、Z的氢化物的稳定性Y<2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃、陶瓷、水泥、光导纤维的化学组成都是硅酸盐 | |
| B. | 污水处理中的化学方法有混凝法、中和法、沉淀法、氧化还原法等 | |
| C. | 对不可回收垃圾常用的处理方法有卫生填埋、堆肥和焚烧 | |
| D. | 固体煤经处理变为气体燃料后,可以减少SO2和烟尘的污染,且燃烧效率高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2 | B. | FeCl3 | C. | O2 | D. | FeCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com