
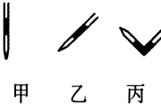 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度进行实验.请填写下列空白:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度进行实验.请填写下列空白:实验编号 | NaOH溶液的浓度/(mol•L-1) | 滴定完成时,NaOH溶液滴入的体积/mL | 待测盐酸的体积/mL |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
分析 (1)①根据配制一定物质的量浓度的溶液的配制步骤完成;
②根据m=nM=cVM来计算;根据称量氢氧化钠固体所需仪器进行解答;
(2)①如溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
②根据滴定消耗的标准液的体积判断数据的有效性,然后计算出标准液的平均体积,最后根据标c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$计算出该盐酸的浓度;
③碱式滴定管的气泡通常橡皮管内,只要将滴定玻璃头朝上,并挤橡皮管中的玻璃珠就可以将气泡冲排出;
④根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差.
解答 解:(1)①配制100mL 0.10mol/L NaOH标准溶液的步骤为:计算→称量→溶解→(冷却后)转移→洗涤(并将洗涤液移入容量瓶)→定容→摇匀→将配制好的溶液倒入试剂瓶中,贴上标签,
故答案为:转移;定容;摇匀;
②需要的氢氧化钠的m=nM=cVM=0.1L×0.10mol•L-1×40g/mol=0.4g;称量0.4g氢氧化钠固体所需仪器,需要称量仪器天平(带砝码、镊子),氢氧化钠具有腐蚀性,应该放在烧杯中称量,还需要取氢氧化钠的仪器药匙;
故答案为:0.4;烧杯(或表面皿);药匙;
(2)①滴定结束前盐酸中滴入酚酞,溶液为无色,滴定结束时氢氧化钠过量,溶液变成红色,所以滴定终点现象为:最后一滴氢氧化钠溶液加入,溶液由无色恰好变成浅红色,且半分钟内浅红色不褪去;
故答案为:最后加入一滴NaOH溶液,溶液由无色恰好变成浅红色且半分钟内浅红色不褪去;
②三次滴定数据都是有效的,消耗标准液的平均体积为:$\frac{22.62+22.72+22.80}{3}$mL=22.713mL,
该盐酸的浓度为:c(HCl)=$\frac{c(NaOH)×V(NaOH)}{V(HCl)}$═$\frac{0.1mol/L×0.022713L}{0.02L}$≈0.11mol/L;
故答案为:0.11mol/L;
③碱式滴定管的气泡通常橡皮管内,只要将滴定玻璃头朝上,并挤橡皮管中的玻璃珠就可以将气泡冲排出;
故答案为:丙;
④A.滴定终点读数时俯视读,造成V(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,可知c(待测)偏小,故A错误;
B.酸式滴定管使用前,水洗后未用待测盐酸润洗,待测液被稀释,其物质的量偏小,造成V(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,可知c(待测)偏小,故B错误;
C.锥形瓶水洗后未干燥,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,可知c(待测)不变,故C错误;
D.滴定前滴定管尖嘴处有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,可知c(待测)偏大,故D正确;
故选D.
点评 本题考查中和滴定操作,题目难度中等,注意把握实验基本方法,能会分析导致误差的不当操作,注意把握实验操作要点和注意事项.


科目:高中化学 来源: 题型:选择题
| A. | 二糖分子中碳原子个数都是葡萄糖的两倍 | |
| B. | 二糖都是由两种单糖组成的混合物 | |
| C. | 二糖水解后都可以得到两种单糖 | |
| D. | 每分子二糖水解后都能生成两分子单糖 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:选择题
下列关于物质的类别的说法不正确的是
A.能在水溶液中或熔融状态下导电的化合物就是电解质
B.胶体是一种能产生丁达尔效应的分散系
C.纯碱不属于碱,干冰属于酸性氧化物
D.Na2O和Na2O2都能与水反应生成对应的碱,它们都是碱性氧化物
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上第一次月考化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃的条件下△H不相同
B.化学反应中的能量变化都表现为热量变化
C.任何放热反应在常温下都能发生
D.化学反应的反应热可通过反应物的键能之和减去生成物的键能之和求得
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高一上9月调研化学试卷(解析版) 题型:选择题
某市对大气进行监测,发现首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。将PM2.5样本用蒸馏水处理制成溶液,该溶液中所含水溶性无机离子的浓度如下表:
离子 | K+ | Na+ | NH4+ | H + | SO42- | NO3- | Cl- |
浓度/mol·L-1 | 4×10-6 | 6×10-6[ | 2×10-5 | x | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断H+ 的浓度为 mol·L-1
A.1×10-5 mol·L-1 B.3×10-5 mol·L-1
C.6×10-5 mol·L-1 D.1×10-4mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
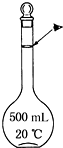 实验室配制500mL 0.5mol•L-1的NaCl溶液,有如下操作步骤:
实验室配制500mL 0.5mol•L-1的NaCl溶液,有如下操作步骤:查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高一上9月调研化学试卷(解析版) 题型:选择题
将下列溶液与1 L 0.1 mol·L-1 NaCl溶液混合,所得溶液c(Cl-)最大的是
A.50 mL 1 mol·L-1 NaCl溶液 B.20 mL 2 mol·L-1 A lCl3溶液
lCl3溶液
C.30 mL 1 mol·L-1 MgCl2溶液 D.100 mL 3 mol·L-1 KClO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com