
| A. | 实验室盛放碳酸钠溶液的试剂瓶不能用玻璃塞 | |
| B. | 泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,使用时只需将两者混合就可产生大量二氧化碳的泡沫 | |
| C. | 用氯化铵溶液除去铁锈 | |
| D. | 可用碳酸钠与醋酸制取少量二氧化碳 |
分析 A.碳酸钠溶液中,碳酸根离子水解,溶液呈碱性,则不能用玻璃塞的试剂瓶盛放碳酸钠溶液;
B.泡沫灭火器利用的是碳酸氢钠与硫酸铝发生双水解反应;
C.氯化铵溶液中,铵根离子水解溶液呈碱性,能够溶液铁锈;
D.醋酸的酸性大于碳酸,则用醋酸与碳酸钠反应制取二氧化碳.
解答 解:A.碳酸钠水解呈碱性,可与二氧化硅反应生成硅酸钠而导致玻璃瓶打不开,实验室盛放碳酸钠溶液的试剂瓶不能用玻璃塞,与水解原理有关,则故A不选;
B.碳酸氢钠溶液和硫酸铝发生互促水解反应而生成二氧化碳气体,可用于灭火,与盐的水解原理有关,故B不选;
C.铵根离子部分水解,溶液呈酸性,氢离子与铁锈反应,该应用与盐的水解原理有关,故C不选;
D.醋酸酸性比碳酸强,可用碳酸钠与醋酸制取少量二氧化碳,与盐类水解无关,故D选;
故选D.
点评 本题考查了盐类水解的应用,为高频考点,题目难度不大,试题侧重于盐的水解原理在生活中的应用的考查,明确盐的水解原理为解答关键,试题培养了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某无色溶液M可能含有离子OH-、HCO3-、CO32-、SO42-、SiO32-、AlO2-、NH4+、MnO4-、Cu2+、Mg2+、Na+、Fe3+中的若干种.取一定量的M溶液滴加盐酸,产生沉淀的物质的量与盐酸体积的关系如图所示(HCO3-与Al3+和AlO2-均要反应,不共存).下列判断正确的是( )
某无色溶液M可能含有离子OH-、HCO3-、CO32-、SO42-、SiO32-、AlO2-、NH4+、MnO4-、Cu2+、Mg2+、Na+、Fe3+中的若干种.取一定量的M溶液滴加盐酸,产生沉淀的物质的量与盐酸体积的关系如图所示(HCO3-与Al3+和AlO2-均要反应,不共存).下列判断正确的是( )| A. | 原溶液中可能含有NH4+、SO42- | |
| B. | 最终溶液中最少含2种溶质 | |
| C. | 原溶液中n(NaAlO2):n(Na2CO3)=1:1 | |
| D. | 滴加盐酸初始阶段发生反应的离子方程式是:CO32-+H+═HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 | |
| B. | 明矾能水解生成Al(OH)3胶体,可用作净水剂 | |
| C. | 沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 | |
| D. | “血液透析”利用了胶体的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
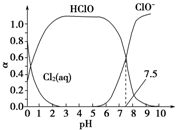 氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强.25℃时氯气-氯水体系中存在以下平衡关系:
氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强.25℃时氯气-氯水体系中存在以下平衡关系:| A. | 由图象可知:Ka=10-7.5 | |
| B. | 在氯处理水体系中,c(HClO)+c(ClO-)>c(H+)-c(OH-) | |
| C. | 用氯处理饮用水时,杀菌效果最佳pH范围为3~6 | |
| D. | 往氯气-氯水体系中加少量碳酸钙,可提高体系漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解水时加入Na2SO4溶液 | |
| B. | 向K2Cr2O7溶液中滴加MaOH溶液后变黄色 | |
| C. | 石灰岩雨水溶蚀形成溶洞 | |
| D. | 用TiCl4与水反应制备TiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com