
【题目】请回答下列问题
(1)H2SO4与HNO3的摩尔质量分别为、 , 9.8g H2SO4与g HNO3所含的分子数相同,它们所含氢原子数之比是 .
(2)一定量H2SO4与HNO3中的氧原子数相等,则溶液中H2SO4与HNO3的物质的量之比为 .
【答案】
(1)98g/mol;63g/mol;6.3;2:1
(2)3:4
【解析】解:(1)摩尔质量以g/mol为单位,数值上等于其相对分子质量,硫酸的相对分子质量为98,所以摩尔质量为:98g/mol,硝酸的相对分子质量为63,所以摩尔质量为63g/mol; 要使硫酸与硝酸分子数相等,依据n= ![]() =
= ![]() 可知,二者物质的量相等,则:
可知,二者物质的量相等,则: ![]() =0.1mol=
=0.1mol= ![]() ,解得硝酸的质量m=6.3g,0.1mol硫酸含有0.2mol氢原子,0.1mol硝酸含有0.1mol氢原子,所以二者所含氢原子数之比是2:1;
,解得硝酸的质量m=6.3g,0.1mol硫酸含有0.2mol氢原子,0.1mol硝酸含有0.1mol氢原子,所以二者所含氢原子数之比是2:1;
所以答案是:98g/mol;63g/mol;6.3;2:1;(2)1个硫酸分子含4个O,1个硝酸分子含有3个O,一定量H2SO4与HNO3中的氧原子数相等,则二者所含氧原子物质的量相等,需满足n(H2SO4)×4=n(HNO3)×3,解得:n(H2SO4):(HNO3)=3:4;
所以答案是:3:4.


科目:高中化学 来源: 题型:
【题目】常温下,向10 mL 0.1 mol·L-1的H2C2O4溶液中逐滴加入0.1 mol·L-1 KOH溶液,所得滴定曲线如图所示。下列说法正确的是( )
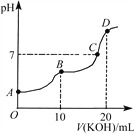
A. KHC2O4溶液呈弱碱性
B. B点时:c(K+)>c(HC2O4-)> c(C2O42-)>c(H+)>c(OH-)
C. C点时:c(K+)>c(HC2O4-)+c(C2O42-)+c(H2C2O4)
D. D点时:c(C2O42-)+c(HC2O4-)+c(H2C2O4)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值)
A. 28g氮气所含有的原子数目为NA
B. 在常温常压下,32克氧气含有的分子数为NA
C. 标准状况下,22.4L水中含有NA个水分子
D. 标准状况下,22.4L氧气和氢气混合物所含的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为25℃时,将0.23 g钠投入到100g水中充分反应,假设反应后溶液体积为100mL,则该溶液的pH为
A. 1 B. 13 C. 12 D. 10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com