
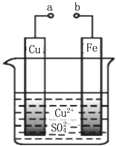
| A. | a和b不连接时,铁片上有红色的铜析出,该装置不能形成原电池 | |
| B. | a和b用导线连接时铜片为负极,发生的反应为:Cu2++2e-═Cu | |
| C. | 无论a和b是否连接,铁片均会被氧化,溶液中均有Fe2+生成 | |
| D. | a和b用导线连接时,溶液中的Cu2+应向铜电极移动 |
分析 a和b不连接时,Fe与硫酸铜溶液发生置换反应,铁能将金属铜从其盐中置换出来;a和b用导线连接时,构成原电池,原电池中,Fe失电子作负极,Cu作正极,正极上铜离子得电子生成铜单质,结合选项分析.
解答 解:A.a和b不连接时,没有形成闭合回路,没有构成原电池,铁把铜置换出来,故A正确;
B.导线连接后,构成原电池,铁比铜活泼,铁作负极,发生的反应为Fe-2e-=Fe2+,故B错误;
C.根据选项A、B分析,无论a和b是否连接,铁片均会被氧化,溶液中均有Fe2+生成,故C正确;
D.构成原电池,阳离子向正极移动,铜作正极,故D正确;
故选B.
点评 本题考查了金属间的置换反应和原电池知识,明确原电池的工作原理及所发生的氧化还原反应是解答本题的关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
| 温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
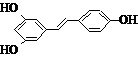 )属二苯乙烯类多酚化合物,具有抗氧化、抗癌和预防心血管疾病的作用.某课题组提出了如下合成路线:
)属二苯乙烯类多酚化合物,具有抗氧化、抗癌和预防心血管疾病的作用.某课题组提出了如下合成路线: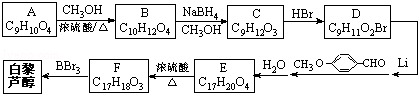

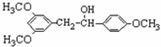 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$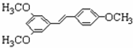 +H2O.
+H2O.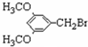 、E
、E .
.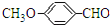 有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:
有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验方法 | |
| A | 检验某混合溶液中是否有Cl- | 取样滴加AgNO3溶液 |
| B | 检验氯化铵中的NH4+ | 加热后,用湿润的红色石蕊试纸靠近试管口 |
| C | 鉴别CO2和SO2 | 分别通入澄清石灰水 |
| D | 检验某试液中是否含有SO42- | 取样滴入盐酸酸化后,再滴入BaCl2溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸的电离方程式:CH3COOH→CH3COO一+H+ | |
| B. | 常温下NH4Cl溶液的pH<7 | |
| C. | 因为SO3的水溶液能够导电,所以SO3是强电解质 | |
| D. | 在常温下的NaOH溶液中,由于NaOH抑制了水的电离,水的离子积常数(KW)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$ Al2O3+3 H2O | B. | 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑ | ||
| C. | FeO+2 HCl═FeCl2+H2O | D. | FeCl2+2NaOH═Fe (OH)2↓+2NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl固体(CaCl2):溶解,加Na2CO3溶液、过滤后加适量盐酸,最后蒸发结晶 | |
| B. | KCl固体(MnO2):溶解、过滤、蒸发结晶 | |
| C. | NaCl溶液(I2):加酒精,萃取、分液 | |
| D. | KNO3溶液(I2):加四氯化碳,萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.结合有关知识,回答下列问题:
乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.结合有关知识,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 分液、蒸馏、萃取 | C. | 萃取、蒸馏、分液 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com