
下列实验现象可用同一原理解释的是
A.品红溶液中分别通入SO2和Cl2,品红均褪色
B.溴水分别滴入植物油和裂化汽油中,溴水均褪色
C.鸡蛋白溶液中分别加入NaCl溶液和HgCl2溶液,均有固体析出
D.分别加热盛有NH4Cl和单质碘的试管,管口均有固体凝结
科目:高中化学 来源: 题型:
近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌的新型高效的多功能水处理剂。高铁酸钾在水处理过程中涉及到的化学过程正确的有 ( )
①蛋白质的变性 ②蛋白质的盐析 ③胶体聚沉 ④盐类水解
⑤焰色反 ⑥氧化还原反应
A.①②③④ B.①③④⑥ C.②③④⑤ D.②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关阿伏加德罗常数(NA)的说法正确的有
A.标准状况下,22.4 L水所含的水分子数为NA
B.0.1mol H2O2催化分解,转移电子数为0.1 NA
C.100mL 0.1mol/L的H2SO3溶液中,含有的离子数约为0.03 NA
D.3.2g Cu与10.0g 98%的H2SO4反应可得0.05NA个SO2气体分子
查看答案和解析>>
科目:高中化学 来源: 题型:
高温油炸食品中常含有害物质丙烯酰胺( )。下列关于丙烯酰胺的叙述错误的是
)。下列关于丙烯酰胺的叙述错误的是
A.属于氨基酸
B.能使酸性KMnO4溶液褪色
C.能发生加聚反应生成高分子化合物
D.与H2N—CH==CHCHO互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学—物质结构与性质】
铜是重要的金属,广泛应用于电气、机械制造、国防等领域,铜的化合物在科学研究和工农业生产中有许多用途。回答下列问题:
(1)Cu原子价层电子排布式为
(2)CuSO4晶体中S原子的杂化方式为 ,SO42-的立体构型为 。
(3)向CuSO4溶液中加入过量氨水,可生成[Cu(NH3)4]SO4,下列说法正确的是
a.氨气极易溶于水,是因为NH3分子和H2O分子之间形成3种不同的氢键
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
 c.[Cu(NH3)4]SO4所含有的化学键有离子键、极性共价键和配位键
c.[Cu(NH3)4]SO4所含有的化学键有离子键、极性共价键和配位键
d.[Cu(NH3)4]SO4组成元素中电负性最大的是氮元素
(4)葡萄糖与新制Cu(OH)2的碱性溶液反应生成砖红色Cu2O沉淀。在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为 ;每个氧原子与 个铜原子配位。
查看答案和解析>>
科目:高中化学 来源: 题型:
RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池,RFC工作原理见图5。下列有关说法正确的是
A.转移0.1mol电子时,a电极产生标准状
况下O2 1.12L
B.b电极上发生的电极反应是:
2H2O+2e-=H2↑+2OH-
C.c电极上进行还原反应,B池中的H+可以
通过隔膜进入A池
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
重铬酸钾(K2Cr2O7)是工业上重要的氧化剂,实验室利用铬铁矿(主要成份为FeO·Cr2O3)模拟工业生产制备重铬酸钾的主要工艺如下:
| |||||||||||||||||
 |  | ||||||||||||||||
|
| ||||||||||||||||
| |||||||||||||||||
 | |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
(1) 铬铁矿中的SiO2和Al2O3在反应器中与纯碱共热反应转变为可溶性盐,写出Al2O3与碳酸钠反应的化学方程式: ▲ 。
|
 6FeO·Cr2O3+24NaOH+7KClO3 12Na2CrO4+3Fe2O3 +7KCl+12H2O。
6FeO·Cr2O3+24NaOH+7KClO3 12Na2CrO4+3Fe2O3 +7KCl+12H2O。
Fe2O3可进一步转化为NaFeO2。NaFeO2在操作Ⅰ中强烈水解,写出NaFeO2水解的化学方程式: ▲ 。
(3)操作Ⅱ的目的是 ▲ 。
(4)操作Ⅲ中CrO42-转化为Cr2O72-,写出此可逆反应的离子方程式:
▲ 。
(5)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于锥形瓶中,加入10mL 2mol·L-1H2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol·L-1Na2S2O3标准溶液滴定至滴定终点时用去Na2S2O3溶液40.00mL(I2+2S2O32-=2I-+S4O62-)。
①写出重铬酸钾与碘化钾反应的离子方程式: ▲ ;
②重铬酸钾试样的纯度(设整个过程中其它杂质不参与反应)为 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学一选修5有机化学基础】(12分)
扑热息痛(学名对乙酸氨基酚)是生活中常用到的一种解热镇痛药。以苯为原料合成扑热息痛的部分转化如下: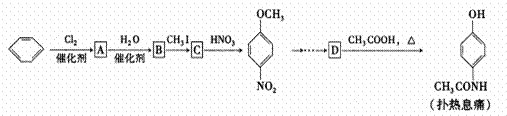
请回答下列问题:
(1)B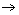 C的反应类型为 ,D中官能团的名称为 。
C的反应类型为 ,D中官能团的名称为 。
(2)C的结构简式为 。
(3)1mol扑热息痛与足量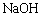 溶液反应,理论上消耗
溶液反应,理论上消耗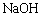 的物质的量为 mol。
的物质的量为 mol。
(4)实验证明B能够与溴水反应,试写出其反应的化学方程式
。
(5)扑热息痛有多种同分异构体,同时符合下列要求的同分异构体有 种。
①苯环上有两个对位取代基;②同于氨基酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
将氯水分别滴入下列溶液,写出观察到的现象及有关反应的离子方程式。
| 观察到的现象 | 反应的离子方程式 | |
| (1)紫色石蕊试液 | ||
| (2)Na2CO3溶液 | ||
| (3)AgNO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com