
【题目】请计算并填空:
(1)含有相同氧原子数的CO和CO2 ,其分子数之比为__________________。
(2))在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,该金属原子的摩尔质量为___________。
(3)48g CH4与标准状况下 ____________L NH3所含H原子个数相等。
(4)在0.4L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,该混合溶液中,含溶质MgCl2的质量为________g;将该混合液加水稀释至体积为1 L,稀释后溶液中Ca2+的物质的量浓度为________mol·L-1。

【答案】 )2:1 24g·mol-1 89.6 19 0.2
【解析】(1)含有相同氧原子数的CO和CO2,其分子数之比为![]() =2:1。(2)在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,则该氯化物的物质的量是0.2mol÷2=0.1mol,摩尔质量是9.5g÷0.1mol=95g/mol,因此该金属原子的摩尔质量为(95-35.5×2)g/mol=24g/mol。(3)48g CH4的物质的量是48g÷16g/mol=3mol,含有12mol氢原子,则相应氨气的物质的量是12mol÷3=4mol,在标准状况下的体积为4mol×22.4L/mol=89.6L。(4)由图可知c(Mg2+)=0.5mol/L,含溶质MgCl2的质量为0.4L×0.5mol/L×95g/mol=19.0g;由电荷守恒可知2c(Ca2+)+c(Na+)+2c(Mg2+)=c(Cl-),解得c(Ca2+)=(3.01.00.5×2)mol/L÷2=0.5mol/L,钙离子的物质的量是0.5mol/L×0.4L=0.2mol,该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为:0.2mol÷1L=0.2mol/L。
=2:1。(2)在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,则该氯化物的物质的量是0.2mol÷2=0.1mol,摩尔质量是9.5g÷0.1mol=95g/mol,因此该金属原子的摩尔质量为(95-35.5×2)g/mol=24g/mol。(3)48g CH4的物质的量是48g÷16g/mol=3mol,含有12mol氢原子,则相应氨气的物质的量是12mol÷3=4mol,在标准状况下的体积为4mol×22.4L/mol=89.6L。(4)由图可知c(Mg2+)=0.5mol/L,含溶质MgCl2的质量为0.4L×0.5mol/L×95g/mol=19.0g;由电荷守恒可知2c(Ca2+)+c(Na+)+2c(Mg2+)=c(Cl-),解得c(Ca2+)=(3.01.00.5×2)mol/L÷2=0.5mol/L,钙离子的物质的量是0.5mol/L×0.4L=0.2mol,该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为:0.2mol÷1L=0.2mol/L。


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】二甲醚CH3OCH3和乙醇CH3CH2OH是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是( )
A.元素分析B.质谱C.红外光谱法D.核磁共振氢谱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中因发生氧化还原反应而不能大量共存的是( )
A. K+、Ba2+、OH-、SO42- B. Cu2+、NH4+、Br-、OH-
C. H+、NO3-、Fe2+、Na+ D. Ag+、Cl-、Fe2+、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() (注:R、R′为烃基)。A为有机合成中间体,在一定条件下发生消去反应,可能得到两种互为同分异构体的产物,其中的一种B可用于制取合成树脂、染料等多种化工产品。A能发生如图所示的变化:
(注:R、R′为烃基)。A为有机合成中间体,在一定条件下发生消去反应,可能得到两种互为同分异构体的产物,其中的一种B可用于制取合成树脂、染料等多种化工产品。A能发生如图所示的变化:
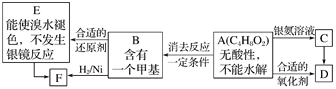
则A的结构简式是( )
A. CH3OHCH=CHCHO B. CH3CH2COOCH3
C. CH3CHOHCH2CHO D. CH2OHCH2CH2CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中的氯离子浓度与50 mL 1 mol·L-1的AlCl3溶液中氯离子浓度相等的是
A. 150 mL 3 mol·L-1的KClO3 B. 75 mL 2 mol·L-1的NH4Cl
C. 350 mL 3 mol·L-1的NaCl D. 150 mL 0.5mol·L-1的CaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果醋是一种由苹果发酵而成的酸性有机饮料,其主要成分是苹果酸。某校化学兴趣小组对苹果醋提纯后得到苹果酸,其结构简式为 。
。
(1)苹果酸分子中所含官能团的名称是_______________、_______________。
(2)苹果酸分子式是_______________。
(3)1 mol苹果酸与足量金属钠反应,可产生_______ mol H2。
(4)1 mol苹果酸与足量NaHCO3溶液反应,可产生_______mol CO2。
(5)氧元素的质量分数为______________。
(6)苹果酸不可能发生的反应有________(填序号)。
①加成反应 ②酯化反应 ③加聚反应
④氧化反应 ⑤消去反应 ⑥取代反应
(7)一定条件下,2 mol苹果酸发生反应,生成1 mol含有八元环的化合物和2 mol H2O,写出反应的化学方程式__________________________________。
(8)该苹果酸有多种同分异构体,写出符合下列条件的同分异构体的结构简式_______________(填写其中一种)。
①在一定条件下,能够发生银镜反应;
②能够与苯甲酸发生酯化反应;
③能够与乙醇发生酯化反应;
④分子中同一碳原子上不存在两个—OH基;
⑤1 mol该酸与足量的金属钠反应产生1.5 mol H2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锑白(Sb2O3)在工业中有着广泛的作用。用辉锑矿(主要成分为Sb2S3,还含有少量 SiO2)制备锑白的工艺流程如下图:

已知:
①Sb3+与Fe2+的氧化性强弱相当。
②Sb2S3不溶于水;Sb2O3为白色粉末,不溶于水,溶于酸和强碱。
③水解时保持溶液的c(H+) =0.1~0.3mol/L。
(1) “浸出”是将辉锑矿溶于FeCl3溶液,为提高浸出速率可采取的措施是_________(任写一种)。请写出其中发生的氧化还原反应离子方程式: _________。滤渣的成分为S单质和_________。
(2) 水解是利用SbCl3的水解反应制取Sb2O3(SbCl3的水解分为多步),其反应可以简单表示为:SbCl3 +3H2O![]() Sb(OH)3 +3HCl,2Sb(OH)3 =Sb2O3 +3H2O。为了促进水解趋于完全,可采取的措施(填两点):_________。
Sb(OH)3 +3HCl,2Sb(OH)3 =Sb2O3 +3H2O。为了促进水解趋于完全,可采取的措施(填两点):_________。
(3) 简述检验沉淀是否洗净的实验方法: _________,若未出现浑浊则证明沉淀己洗干净,反之则没有。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化需克服相同类型作用力的是( )。
A. 碘和干冰的升华 B. Na2O2和C60的熔化
C. 氯化氢和氯化钾的溶解 D. 溴的气化和NH4Cl加热分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学反应与能量的说法正确的是
A. 燃烧属于放热反应 B. 中和反应是吸热反应
C. 形成化学键时吸收能量 D. 反应物总能量与生成物总能量一定相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com