
【题目】硫化氢是一种有臭鸡蛋气味的剧毒气体,在生产、生活及科研中均有重要应用。
(1)工业上采用高温热分解H2S的方法制取H2,在膜反应器中分离出H2,发生的反应为2H2S(g)![]() 2H2(g)+S2(g)△H
2H2(g)+S2(g)△H
已知:①H2S(g)![]() H2(8)+S(g)△H1
H2(8)+S(g)△H1
②2S(g)![]() S2(g)△H2
S2(g)△H2
则△H=________(用含△H1、△H2的式子表示)。
(2)在容积2 L的恒容密闭容器中,控制不同温度进行H2S分解:2H2S(g)![]() 2H2(g)+S2(g)。H2S的起始物质的量均为1mol,实验过程中测得H2S的转化率如图1所示。曲线a表示H2S的平衡转化率与温度的关系,曲线b表示不同温度下反应经过相同时间时H2S的转化率。
2H2(g)+S2(g)。H2S的起始物质的量均为1mol,实验过程中测得H2S的转化率如图1所示。曲线a表示H2S的平衡转化率与温度的关系,曲线b表示不同温度下反应经过相同时间时H2S的转化率。

①反应2H2S (g)![]() 2H2(g)+S2(g)是放热还是吸热,判断并说理由________。
2H2(g)+S2(g)是放热还是吸热,判断并说理由________。
②随着H2S分解温度的升高,曲线b向曲线a逐渐靠近,其原因是________ 。
③在985℃时,该反应经过5 s达到平衡,则该反应的平衡常数为________。在图2中画出985℃时,0~6s 体系中S2(g)浓度随时间的变化曲线。___________________


(3)工业上常用NaOH溶液吸收H2S废气,吸收后所得溶液进行电解(装置如图3所示),在阳极区可生成Sx2-,写出生成Sx2-离子的电极反应式:________。
【答案】 2△H1+△H2 吸热反应,H2S的平衡转化率随温度的升高而逐渐增大 温度升高,反应速率加快,达到平衡所需时间缩短 0.044 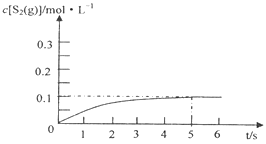 xS2--2(x-1)e-=Sx2-或[S2--2e-=S↓,(x-1)S+S2-=Sx2-
xS2--2(x-1)e-=Sx2-或[S2--2e-=S↓,(x-1)S+S2-=Sx2-
【解析】(1)本题考查热化学反应方程式的计算,①×2-②得出△H=2△H1-△H2;(2)本题考查勒夏特列原理、影响化学反应速率的因素、化学平衡常数的计算,①根据图像,随着温度的升高,H2S的转化率增大,根据勒夏特列原理,正反应为吸热反应;②温度升高,化学反应速率加快,达到平衡所用时间缩短;③2H2S(g)![]() 2H2(g)+S2(g)
2H2(g)+S2(g)
起始: 1 0 0
变化:0.4 0.4 0.2
平衡:0.6 0.4 0.2 根据化学平衡常数的表达式K=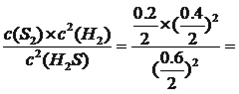 0.044;S2的物质的量随着时间增加而增加,在5s达到平衡,此时S2的浓度为0.2/2mol·L-1=0.1mol·L-1,即图像为
0.044;S2的物质的量随着时间增加而增加,在5s达到平衡,此时S2的浓度为0.2/2mol·L-1=0.1mol·L-1,即图像为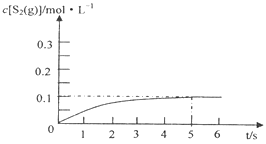 ;(3)本题考查电极反应式的书写,根据图3,电极b产生氢气,电极反应式为2H++2e-=H2↑,电极b为阴极,电极a为阳极,阳极上产生Sx2-,电极a电极反应式为xS2--2(x-1)e-=Sx2-。
;(3)本题考查电极反应式的书写,根据图3,电极b产生氢气,电极反应式为2H++2e-=H2↑,电极b为阴极,电极a为阳极,阳极上产生Sx2-,电极a电极反应式为xS2--2(x-1)e-=Sx2-。


科目:高中化学 来源: 题型:
【题目】三氯氧磷(POCl3)常用作半导体掺杂剂及光导纤维原料。某化学小组用PCl3氧化法制备POCl3的装置如下图所示。已知:POCl3的沸点是105.1℃,PCl3 的沸点是65.5℃;二者遇潮湿空气都易生成酸雾。

(1)仪器a的名称为_______________。
(2)装置A是氧气的发生装置,试写出A中发生反应的化学方程式:___________________。
(3)装置B的作用是______________________________________________________________。
(4)装置C中反应温度应控制在60~65℃,原因是_____________________________________。
(5)通过佛尔哈德法可以测定POCl3产品中氯元素的质量分数,实验步骤如下:
Ⅰ.取1.5000g 产品于锥形瓶中,加入足量NaOH溶液,待完全水解后加稀硝酸调至酸性。
Ⅱ.向锥形瓶中加入3.2000mol·L-1的AgNO3溶液10.00mL,使Cl-完全沉淀。
Ⅲ.向其中加入2.00mL硝基苯,用力摇动,使沉淀表面被硝基苯覆盖。
Ⅳ.加入指示剂,用0.2000mol·L-1NH4SCN标准溶液滴定过量Ag+至终点,消耗10.00mLNH4SCN溶液。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2.0×10-12。
①滴定选用的指示剂是________(填代号)。
a.FeCl2 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②实验过程中加入硝基苯的目的是_____________________________,若无此操作所测氯元素的质量分数将会________(填“偏大”、“偏小” 或“不变”)。
③产品中氯元素的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~H分别表示中学化学中常见的某种物质,它们之间的相互转化关系如下图所示(部分反应物、生成物未列出)。已知:C、D、E、F、G五种物质中均含有同一种元素;A为淡黄色固体化合物;G为红褐色固体。

(1)写出化学式:A:________________;C:________________;F:________________。
(2)写出反应的化学方程式:
②_____________________________________________________________。
⑥_____________________________________________________________。
(3)写出离子方程式:
③_____________________________________________________________。
⑤_____________________________________________________________。
(4)生成24 g B需要转移________mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 11gC3H8与CO2的混合气体中所含碳原子数可能为0.5NA
B. 标准状况下,4.48L甲烷和乙烯的混合气体完全燃烧,产物中所含O-H键数目为0.4NA
C. 4.6gNa与100mL1mol·L-1的盐酸溶液反应,转移电子数目为0.1NA
D. 常温下,1LpH=2的硫酸溶液中由水电离出的H+的数目为0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,体积均为0.25 L的三个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1,达到平衡。下列说法正确的是( )
2NH3(g) ΔH=-92.4 kJ·mol-1,达到平衡。下列说法正确的是( )
容器编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | ||
N2 | H2 | NH3 | NH3 | ||
① | 500 | 1 | 3 | 0 | 0.5 |
② | 500 | 0.6 | 1.8 | 0 | |
③ | 550 | 0 | 0 | 2 | a |
A. 容器①、②中反应的平衡常数不相等
B. 达平衡时,容器②中H2的转化率大于25%
C. a<0.5
D. 起始时向容器①中充入1 mol N2、2 mol H2、0.5 mol NH3,则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家积极探索新技术对CO2进行综合利用。请回答下列问题:
(1)已知: H2的燃烧热为285.8kJ/mol,C2H4的燃烧热为1411.0kJ/mol,且H2O(g)=H2O(l)ΔH=-44.0kJ/mol,则CO2 和H2反应生成乙烯和水蒸气的热化学方程式为____________,上述反应在__________下自发进行(填“高温”或“低温”)。
(2)乙烯是一种重要的气体燃料,可与氧气、熔融碳酸钠组成燃料电池。写出该燃料电池负极的电极反应式:_______________________.
(3)在体积为1L的密闭容器中,充入3mol H2和1mol CO2,测得温度对CO2的平衡转化率和催化剂催化效率的影响如图所示。
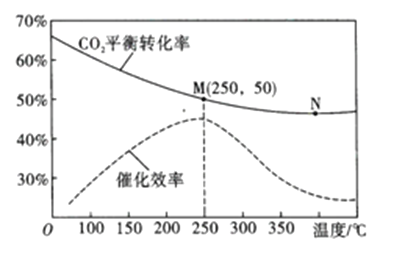
①平衡常数: KM__________KN (填“>”“<”或“=”)。
②下列说法正确的是_________(填序号)。
A.当混合气体密度不变时,说明反应达到平衡状态
B.当压强或n(H2)/n(CO2)不变时,均可证明反应已达平衡状态
C.当温度高于250℃时,因为催化剂的催化效率降低,所以平衡向逆反应方向移动
D.若将容器由“恒容”换为“恒压”,其他条件不变,则CO2的平衡转化率增大
③250℃时,将平衡后的混合气体(不考虑平衡移动) 通入300mL 3mol/L的NaOH溶液中充分反应,则所得溶液中所有离子的浓度大小关系为__________
④图中M点对应乙烯的质量分数为_____________。
(5)达平衡后,将容器体积瞬间扩大至2L并保持不变,平衡向_____移动(填“正向”“逆向”或“不”),容器内混合气体的平均相对分子质量______(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化如图所示。已知W的一种核素的质量数为18,中子数为10;X是短周期元素中原子半径最大的;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法不正确的是

A. 简单离子半径:W>X>Z
B. 最简单气态氢化物的稳定性:Y<Z
C. 化合物XZW中既含离子键又含共价键
D. Y的氧化物能与X的最高价氧化物对应的水化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA代表阿伏加德罗常数,则关于热化学方程式 C2H2 (g) +5/2O2 (g) →2CO2 (g)+H2O(l) △H = —1300kJ / mol 的说法中,正确的是 ( )
A. 当8 NA个电子转移时,该反应放出1300kJ的能量
B. 当1 NA个水分子生成且为液体时,吸收1300kJ的能量
C. 当2 NA个碳氧共用电子对生成时,放出1300kJ的能量
D. 当8 NA个碳氧共用电子对生成时,放出1300kJ的能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com