
未来新能源的特点是资源丰富,在使用时对环境无污染或者污染很小,且可以再生。下列属于未来新能源标准的是
①天然气 ②生物质能 ③潮汐能 ④石油 ⑤太阳能 ⑥煤 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧ C.③④⑤⑥⑦⑧ D.②③⑤⑦⑧
科目:高中化学 来源:2016-2017学年山西太原五中高二12月阶段测文化学卷(解析版) 题型:选择题
我国卫生部 门制定的《关于宣传吸烟有毒与控制吸烟》的通知中规定:“中学生不准吸烟”。香烟
门制定的《关于宣传吸烟有毒与控制吸烟》的通知中规定:“中学生不准吸烟”。香烟 燃烧产生的烟气中,有多种有害物质,其中尼古丁(C10H14N2)对人体危害最大,下列说法正确的是
燃烧产生的烟气中,有多种有害物质,其中尼古丁(C10H14N2)对人体危害最大,下列说法正确的是
A.尼古丁是由26个原子构成的物质
B.尼古丁中C、H、O 三种元素的质量比为10:14:2
C.尼古丁的相对分子质量是162g
D.尼古丁中氮元素的 质量分数为17.3 %
质量分数为17.3 %
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省宜春市高一上月考二化学卷(解析版) 题型:选择题
下列有关物质制备的反应中,其原理不属于氧化还原反应的是( )
A.制金属钛 B.湿法炼铜 C.实验室制O2 D.侯氏制碱
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省宜春市高二上月考二化学卷(解析版) 题型:选择题
已知反应AsO43-+2I-+2H+ AsO33-
AsO33- +I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
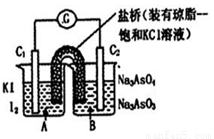
Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液
结果发现电流计指针均发生偏转.据此,下列判断正确的是
A.Ⅰ操作过程中,C2棒上发生的反应为:AsO43-+2H++2e-=AsO33-+H2O
B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液
C.操作Ⅰ过程中,C1为正极
D.Ⅱ操作过程中,C1棒上发生的反应为:2I-_2e-=I2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省宜春市高二上月考二化学卷(解析版) 题型:选择题
同温同压下,下列各组热化学方程式中,△H1<△H2是
A.C(s)+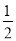 O2(g)=CO(g);△H1 C(s)+O2(g)=CO2(g);△H2
O2(g)=CO(g);△H1 C(s)+O2(g)=CO2(g);△H2
B.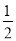 H2(g
H2(g )+
)+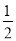 Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2
Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2 HCl(g);△H2
HCl(g);△H2
C.S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g); △H2
D.2H2(g)+O2(g)=2H2O(g);△H1 2H2(g)+O2(g)=2H2O(l);△H2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省饶阳县高一上期中化学试卷(解析版) 题型:填空题
(1)0.3mol NH3分子中所含原子数与__________个H2O分子中所含原子数相等.
(2)含0.4mol A13+的Al2(SO4)3中所含的SO42﹣的物质的量是__________.
(3)已知16g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为__________.
(4)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是__________.
(5)某盐混合溶液中含有离子:Na+、Mg2+、Cl﹣、SO42﹣,测得Na+、Mg2+ 和Cl﹣的物质的量浓度依次为:0.2mol•L﹣1、0.25mol•L﹣1、0.4mol•L﹣1,则c(SO42﹣)=__________.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省饶阳县高一上期中化学试卷(解析版) 题型:选择题
燃着的镁条在下列气体中不能继续燃烧的是( )
A.CO2 B.N2 C.Cl2 D.He
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一上期中化学卷(解析版) 题型:实验题
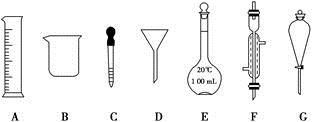
(1)写出仪器名称:D________,F________。
(2)下列实验操作中用到仪器G的是________(填下列选项的编号字母)。]
a.分离水和CCl4的混合物 b.分离水和酒精的混合物 c.分离水和泥沙的混合物
(3)实验室需要配制450mL 0.4 mol/L的硫酸溶液。
①配制时,实验室提供了以下仪器:烧杯、100mL量筒、玻璃棒、托盘天平(带砝码)、胶头滴管,还缺少的玻璃仪器是 。上述实验中使用容量瓶前必须进行的操作是
②配制该溶液需用98﹪的浓硫酸(密度为1.8g/mL)___________mL。取用该体积浓硫酸时,需要用到上述仪器中的A和___________(填仪器的编号字母)。
③下列操作会使配制的溶液浓度偏高的是________(填下列选项的编号字母)。
A.转移过程中有少量溶液溅出 |
B.没有冷却,立即转移到容量瓶中定容 |
C.摇匀后,液面下降,补充水 |
D.定容时俯视刻度线 |
E.量筒量取浓硫酸是仰视刻度线
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长株潭岳益五市十校高三12月联考化学卷(解析版) 题型:实验题
高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂。工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如下:
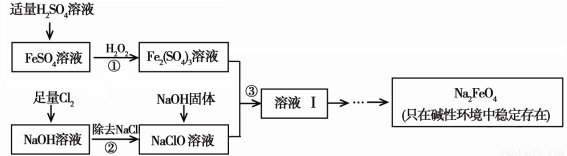

(1)高铁酸钠中铁元素的化合价为 ,次氯酸钠的电子式是________。
(2)步骤①反应的离子方程式是 。
(3)从溶液I中分离出Na2FeO4后,还有副产品Na2SO4 、NaCl,则步骤③中反应的离子方程式为 。
(4)工业上还可用电解浓NaOH溶液的方法制Na2FeO4,其工作原理如图所示:
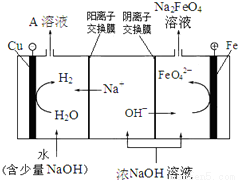
阳极的电极反应式为 。可循环使用的物质是 。
(5)计算Na2FeO4的消毒效率(以单位质量得到的电子数表示)约是氯气的________倍,
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com