
【题目】一种特殊的热激活电池示意图如下。该电池总反应为:PbSO4(s)+2LiCl+Ca(s)= CaCl2(s)+ Li2SO4+Pb(s) ,下列说法不正确的是
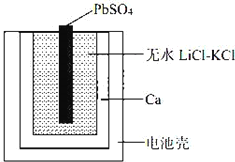
A. Ca电极发生氧化反应
B. 负极的电极反应:Ca(s)+2Cl﹣﹣2e﹣= CaCl2(s)
C. 可用 LiCl 和 KCl 水溶液代替无水 LiCl﹣KCl
D. 当无水LiCl﹣KCl混合物受热熔融后电池才能工作
【答案】C
【解析】
由原电池总反应可知Ca失电子为原电池的负极,被氧化生成CaCl2,负极的电极反应式为Ca+2Cl--2e-=CaCl2,PbSO4为原电池的正极,发生还原反应,电极反应式为PbSO4+2e-+2Li+=Li2SO4+Pb,结合原电池原理分析解答。
A.根据原电池总反应可知Ca失电子为原电池的负极,发生氧化反应,故A正确;
B.Ca为原电池的负极,被氧化生成CaCl2,电极反应式为Ca(s)+2Cl﹣﹣2e﹣= CaCl2(s),故B正确;
C.Ca是活泼金属,能与水直接反应,所以不能用水溶液作电解质,故C错误;
D.无水LiCl﹣KCl常温为固体,不能导电,需要将无水LiCl﹣KCl混合物受热熔融,该原电池才能工作,故D正确;
答案选C。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】铁及其化合物广泛存在于人们的日常生活和工业生产中。回答下列问题:
(1)基态Fe原子的核外电子排布式是________,Ca元素与Fe元素同周期,灼烧![]() ,火焰为砖红色,节日中燃放的焰火配方中常含有Ca元素,灼烧Ca元素呈现特殊颜色的原因是____
,火焰为砖红色,节日中燃放的焰火配方中常含有Ca元素,灼烧Ca元素呈现特殊颜色的原因是____
(2)人体内血红蛋白的结构简式如图所示:
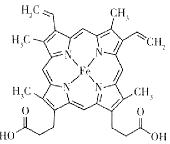
①组成血红蛋白的5种元素中,电负性由大到小的顺序是_________,C、N、O的第一电离能由大到小的顺序是_______。
②血红蛋白分子结构中N的杂化方式是_______。
③血红蛋白分子结构中含有配位键,为这些配位键提供孤电子对的元素是_______(写元素符号,下同),提供空轨道的元素是______。
(3)![]() 可应用于工业生产中的催化剂,其晶胞结构如图所示:
可应用于工业生产中的催化剂,其晶胞结构如图所示:
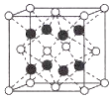
①已知电负性:Fe-1.83,Br-2.96,则![]() 中含有的化学键类型为_________。
中含有的化学键类型为_________。
②![]() 晶胞中铁的配位数是_________;
晶胞中铁的配位数是_________;![]() 晶胞边长为a cm,则
晶胞边长为a cm,则![]() 晶体密度的表达式为_____________
晶体密度的表达式为_____________![]() (设阿伏加德罗常数的值为NA)。
(设阿伏加德罗常数的值为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,某化学兴趣小组设计了一个燃料电池,并探究氯碱工业原理和粗铜精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:

(1)通入氧气的电极为_____(填“正极”或“负极”),此电极反应式为_________。
(2)铁电极为_______(填“阳极”或“阴极”),乙装置中电解反应的化学方程式为_________________。
(3)某粗铜中含有铁、金、银和铂等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如下工艺流程:
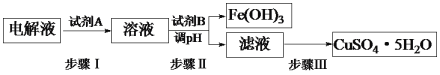
已知:几种金属阳离子开始沉淀和沉淀完全的pH。
氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
Fe3+ | 1.9 | 3.2 |
Fe2+ | 7.6 | 9.6 |
Cu2+ | 4.7 | 6.7 |
①步骤I中加入试剂A的目的是_____________________________,试剂A应选择______(填序号);
a.氯气 b.过氧化氢 C.酸性高锰酸钾溶液
②步骤II中试剂B为_________(答出一种即可),调节pH的范围是___________;
③步骤III的操作是加热浓缩、___________、过滤。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁电池因具有高的安全性和低廉的价格而备受关注,我国科学 家最近研发出一种新型镁电池,其工作原理如图所示。下列说法正确的是

A.I 室中的电解质溶液可以是稀 H2SO4
B.外电路中转移 2mol 电子时,N 极质量增加 24a g
C.离子交换膜为阳离子交换膜
D.电子流向:M 电极→I 室→离子交换膜→II 室→N 极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的X加入某密闭容器中,发生反应:2X(g)![]() 3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断不正确的是( )
3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断不正确的是( )

A.升高温度,该反应平衡常数K增大
B.压强大小有P3>P2>P1
C.反应过程中加入高效催化剂可以缩短达到平衡的时间
D.在该条件下M点X平衡转化率为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对甲基苯乙酮是重要的化工原料,某实验小组利用如图装置制备对甲基苯乙酮。

制备原理: (放热反应)。 反应物和产物的相关数据列表:
(放热反应)。 反应物和产物的相关数据列表:
试剂名称 | 分子式 | 分子量 | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 |
甲苯 | C7H8 | 92 | -93 | 110.6 | 0.8669 |
乙酸酐 | (CH3CO)2 | 102 | -73.1 | 138.6 | 1.08 |
对甲基苯乙酮 | C9H10O | 134 | 28 | 94(0.93kPa) | 1.0051 |
实验步骤:
步骤 1:如图所示,在 100mL 三颈烧瓶上安装搅拌器、仪器 x 和上口装有无水氯化钙的冷凝管,干燥管与一气体 吸收装置相连。
步骤 2:三颈烧瓶中快速加入研碎的催化剂和 20mL 无水甲苯,在搅拌的条件下通过仪器 x 缓慢地滴加 3.4mL 醋酸酐与 5mL 甲苯的混合液,约需 15min 滴完。
步骤 3:反应结束后,将三颈烧瓶在 95℃时加热 25~30min。
步骤 4:反应混合液冷却后转移到盛有 30mL 浓盐酸与 30mL 冰水的烧杯中(目的是将对甲基苯乙酮从其与铝的化 合物中分离出来),用分液漏斗分出有机层、水层。每次用 5mL 甲苯萃取两次,并将所有甲苯层合并,然后依次 用水、10%氢氧化钠溶液、水各 10mL 洗涤有机层,最后用无水硫酸镁处理。
步骤 5:将干燥后的溶液滤入蒸馏瓶,减压蒸馏(整套装置必须是干燥的),收集 94℃(0.93kPa)馏分,得到对甲 基苯乙酮 4.1g。
请回答下列问题:
(1)仪器 x 的名称为________。与普通的分液漏斗相比,本实验采用仪器 x 的优点为_______。
(2)本实验中的氯化铝若水解则会影响催化效率,除了使用干燥管的措施外,还应该采取哪些措施防止水解_____(答两点)。
(3)步骤③中最适宜的加热方式为 _____。
(4)步骤④中加入 10%的氢氧化钠溶液的目的为 _____,加入无水硫酸镁的目的为_________。
(5)步骤④中水层每次用 5mL 甲苯萃取两次并将所有甲苯层合并的目的为________。
(6)步骤⑤中减压蒸馏时所需的冷凝装置能否选用题给装置图中的球形冷能管_____(答“能”或“不能”)。 本实验中,对甲基苯乙酮的产率为_____(结果保留 2 位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄色固体聚合硫酸铁(SPFS)是一种重要的无机高分子絮凝剂,极易溶于水,作为工业和生活污水处理等领域具有重要的应用。SPFS可表示成Fex(OH)y(SO4)z·nH2O。工业上常用的一种制备流程为:(绿矾化学式为FeSO4·7H2O)
![]()
在SPFS的多个质量指标中,盐基度是重要的质量指标之一,盐基度定义为:盐基度=n(OH-)/3n( Fe) ×100%。式中n(OH-)、n(Fe)分别表示固体聚合硫酸铁中OH一和Fe的物质的量。试回答下列问题。
(1)在绿矾中加人酸性介质的NaClO3目的是__________ 。
(2)SPFS溶于水后并与水反应生成__________ 能吸附水中的悬浮物来净化水。
(3)取15.05g某固体聚合硫酸铁溶解于水,向其中加人过量的BaCI2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀20.97g.向上述滤液中加人NH3H2O,调节溶液pH= 6,经过滤、洗涤、干燥得Fe2O3固体5.60g。该固体聚合硫酸铁的盐基度为_________ 。
(4)计算出该固体聚合硫酸铁样品的化学式______________(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,将SO2通入NaOH溶液得到一组c(H2SO3)+c(HSO3-)+c(SO32-)=0.100 mol·L-1的混合溶液,溶液中部分微粒的物质的量浓度随pH的关系曲线如右下图所示。下列叙述正确的是
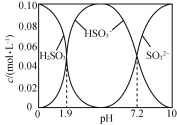
A.H2SO3的Ka2=10-7.2
B.pH=1.9的溶液中:c(Na+)>c(H2SO3)=c(HSO3-)> c(SO32-)
C.c(Na+)=0.100 mol·L-1的溶液中:c(H+)+c(SO32-)=c(OH-)+c(H2SO3)
D.c(HSO3-)=0.050 mol·L-1的溶液中:c(H+)+c(Na+)<0.150 mol·L-1+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铬绿(Cr2O3)的性质独特,在冶金、颜料等领域有着不可替代的地位。一种利用淀粉水热还原铬酸钠(Na2CrO4)制备氧化铬绿的工艺流程如下:
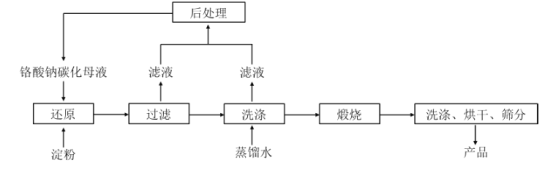
已知:①向含少量 Na2 CO3的铬酸钠碱性溶液中通入CO 2可制得不同碳化率的铬酸钠碳化母液;
②“还原”反应剧烈放热,可制得 Cr(OH) 3 浆料。
(1)铬酸钠(Na2CrO4)中铬元素的价态是________,该工艺中“还原”反应最初使用的是蔗糖或甲醛,请写出甲醛的电子式:________________,后来改用价格低廉的淀粉。请写出甲醛(HCHO)与铬酸钠(Na2CrO4)溶液反应的离子方程式___________________________ 。
(2)将混合均匀的料液加入反应釜,密闭搅拌,恒温发生“还原”反应,下列有关说法错误的是____________(填标号)。
A.该反应一定无需加热即可进行 B.必要时可使用冷却水进行温度控制
C.铬酸钠可适当过量,使淀粉充分反应 D.应建造废水回收池,回收含铬废水
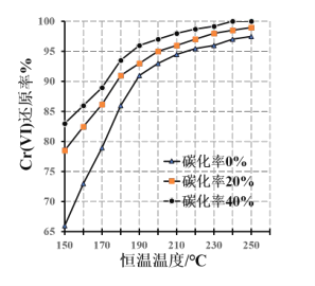
(3)测得反应完成后在不同恒温温度、不同碳化率下 Cr(Ⅵ)还原率如下图。实际生产过程中 Cr(Ⅵ)还原率可高达 99.5%以上,“还原”阶段采用的最佳反应条件为________________。
(4)滤液中所含溶质为_________________。该水热法制备氧化铬绿工艺的优点有________________ 、___(请写出两条)。
(5)重铬酸钠(Na2Cr2O7·H2O)与硫酸铵热分解法也是一种生产氧化铬绿的方法,生产过程中产生的气体对环境无害,其化学反应方程式为______________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com