
(18分)研究氮的固定具有重要意义。
(1)雷雨天气中发生自然固氮后,氮元素转化为________而存在于土壤中。处于研究阶段的化学固定
新方法是N2在催化剂表面与水发生如下反应:
2N2(g)+6H2O(l)=4NH3(g)+3O2(g) △H K ①
已知:N2(g)+3H2(g)=2NH3(g) △H1=-92.4kJ·mol-1 K1 ②
2H2(g) +O2(g) =2H2O(l) △H2=-571.6kJ·mol-1 K2 ③
则△H =________;K=___________(用K1和 K2表示)。
(2)在四个容积为2L的密闭容器中,分别充入1mol N2、3mol H2O,在催化剂条件下进行反应①3h,实验数据见下表:
序号 | 第一组 | 第二组 | 第三组 | 第四组 |
t/℃ | 30 | 40 | 50 | 80 |
NH3生成量/(10﹣6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
下列能说明反应①达到平衡状态的是_____(填字母)。
a.NH3和O2的物质的量之比为4∶3
b.反应混合物中各组份的质量分数不变
c.单位时间内每消耗1molN2的同时生成2molNH3
d.容器内气体密度不变
若第三组反应3h后已达平衡,第三组N2的转化率为___________;第四组反应中以NH3表示的反应速率是__________________,与前三组相比,NH3生成量最小的原因可能是_________________。
(3)美国化学家发明一种新型催化剂可以在常温下合成氨,将其附着在电池的正负极上实现氮的电化学固定,其装置示意图如下:
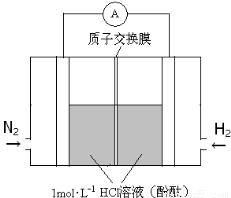
则开始阶段正极反应式为_____________;忽略电解过程中溶液体积变化,当电池中阴极区溶液pH = 7时,溶液中NH3·H2O的浓度为___________( Kb=2×10-5mol·L-1);当电池中阴极区呈红色时,溶液中离子浓度由大到小的顺序为_________________。
(1)硝酸盐或NO3- (合理答案即给分1分) +1530kJ· mol-1(2分) K12/K23(2分) (2)bd(2 分)3×10-4%(2分) 3.33×10﹣7mol·(L·h)-1(2分)催化剂在80℃活性减小,反应速率反而减 慢(1分) (3)N2+8H++6e-= 2NH4+(2分)5×10-3mol·L-1(2分)c(NH4+)>c(Cl-)>c(OH-)>c(H+)(2分)
【解析】
试题分析:(1)雷雨天气中发生自然固氮反应是O2 +N2 2NO,生成的NO与空气中的氧气反应生成NO2,NO2溶于水转变为HNO3,所以氮元素转化为最后硝酸盐或NO3-而存在于土壤中;将②×2-③×3可得①,则△H =-92.4×2+571.6×3=+1530kJ· mol-1,根据三个式子的关系则K=K12/K23。(2)反应达到平衡状态的两个根本标志是:各物质的浓度不再变化、同种物质的消耗速率和生成速率相等。a.NH3和O2的物质的量之比为4∶3,不能说明NH3和O2的浓度不再改变,错; b.反应混合物中各组份的质量分数不变,说明各物质的质量不变,浓度也就不变,对;c.不管在任何时候单位时间内每消耗1molN2的同时生成2molNH3,不能判断是否达到了平衡,错;d. 由于H2O液态。反应没有达到平衡,气体的质量会发生改变,如果容器内气体密度不变,说明气体的消耗和生成速率相等,说明反应达到了平衡,对;选bd。根据方程式知道生成6.0×10﹣6mol的NH3要消耗3.0×10﹣6mol的N2,则N2的转化率为:(3.0×10﹣6)/1 ×100%=3×10-4%。第四组反应中生成了2.0×10﹣6mol 的NH3,则以NH3表示的反应速率是2.0×10﹣6÷2L÷3h= 3.33×10﹣7mol·(L·h)-1,第四组反应温度较高,反应时间相同但生成的NH3较少,最有可能是在该温度下催化剂的催化效果降低了,使得反应变慢了。(3)正极反应的物质得到电子化合价降低,所以N2在正极反应,由于是酸性介质生成的NH3会转变为NH4+,则电极反应为:N2 + 8H+ + 6e-= 2NH4+;由于盐酸的浓度为1mol/L,当溶液为中性的时候c(NH4+)约为1mol/L,则c(NH3·H2O)= c(NH4+)·c(OH-)/ Kb = 10-7/(2×10-5 )= 5×10-3mol·L-1。当电池中阴极区呈红色时溶液显碱性,NH3·H2O较多,所以溶液中离子浓度由大到小的顺序为c(NH4+)>c(Cl-)>c(OH-)>c(H+)。
2NO,生成的NO与空气中的氧气反应生成NO2,NO2溶于水转变为HNO3,所以氮元素转化为最后硝酸盐或NO3-而存在于土壤中;将②×2-③×3可得①,则△H =-92.4×2+571.6×3=+1530kJ· mol-1,根据三个式子的关系则K=K12/K23。(2)反应达到平衡状态的两个根本标志是:各物质的浓度不再变化、同种物质的消耗速率和生成速率相等。a.NH3和O2的物质的量之比为4∶3,不能说明NH3和O2的浓度不再改变,错; b.反应混合物中各组份的质量分数不变,说明各物质的质量不变,浓度也就不变,对;c.不管在任何时候单位时间内每消耗1molN2的同时生成2molNH3,不能判断是否达到了平衡,错;d. 由于H2O液态。反应没有达到平衡,气体的质量会发生改变,如果容器内气体密度不变,说明气体的消耗和生成速率相等,说明反应达到了平衡,对;选bd。根据方程式知道生成6.0×10﹣6mol的NH3要消耗3.0×10﹣6mol的N2,则N2的转化率为:(3.0×10﹣6)/1 ×100%=3×10-4%。第四组反应中生成了2.0×10﹣6mol 的NH3,则以NH3表示的反应速率是2.0×10﹣6÷2L÷3h= 3.33×10﹣7mol·(L·h)-1,第四组反应温度较高,反应时间相同但生成的NH3较少,最有可能是在该温度下催化剂的催化效果降低了,使得反应变慢了。(3)正极反应的物质得到电子化合价降低,所以N2在正极反应,由于是酸性介质生成的NH3会转变为NH4+,则电极反应为:N2 + 8H+ + 6e-= 2NH4+;由于盐酸的浓度为1mol/L,当溶液为中性的时候c(NH4+)约为1mol/L,则c(NH3·H2O)= c(NH4+)·c(OH-)/ Kb = 10-7/(2×10-5 )= 5×10-3mol·L-1。当电池中阴极区呈红色时溶液显碱性,NH3·H2O较多,所以溶液中离子浓度由大到小的顺序为c(NH4+)>c(Cl-)>c(OH-)>c(H+)。
考点:反应热的计算、化学平衡状态的判断、反应速率的计算、电极反应的书写、离子浓度的计算和大小比较。
考点分析: 考点1:化学反应与能量 考点2:化学平衡状态及移动 考点3:原电池 试题属性

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源:2014-2015学年北京市海淀区高三年级3月适应性训练理综化学试卷(解析版) 题型:推断题
(14分)醋硝香豆素是一种治疗心脑血管疾病的药物,能阻碍血栓扩展,其结构简式为:

醋硝香豆素可以通过以下方法合成(部分反应条件省略)。

已知: + H2O
+ H2O
回答以下问题:
(1)反应①的反应类型是 。
(2)从A到B引入的官能团名称是 。
(3)反应②的化学方程式为 。
(4)反应③的化学方程式为 。
(5)关于E物质,下列说法正确的是 (填字母序号)。
a.在核磁共振氢谱中有四组吸收峰
b.可以用酸性高锰酸钾溶液鉴别D和E
c.可以发生加成反应、聚合反应、氧化反应和还原反应
d.存在顺反异构
(6)写出G的结构简式 。
(7)分子结构中只含有一个环,且同时符合下列条件的G的同分异构体共有 种。
①可与氯化铁溶液发生显色反应;②可与碳酸氢钠溶液反应生成二氧化碳气体。其中,苯环上的一氯代物只有两种的同分异构体的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三上学期期末考试化学试卷(解析版) 题型:填空题
(10分)将E 和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)  2G(g)。
2G(g)。
若忽略固体体积,平衡时 G 的体积分数随温度和压强的变化如下表所示。请填写下列空格:

(1)表中数据b f。(选填“>”、“<”或“=”)
(2)该反应的熵变ΔS 0,ΔH 0。(选填“>”、“<”或“=”)
(3)根据表中数据,可计算求得915℃、2.0MPa时E 的转化率为 。
(4)上述反应达到平衡后,若保持体系温度不变,下列措施中能提高混合体系中气体E的体积分数的是
A.保持容器容积不变,充入一定量的气体 E
B.保持容器内压强不变,充入一定量的气体 G
C.加入少量固体F的粉末
D.保持容器容积不变,同时充入一定量的气体 E 和G
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三上学期期末考试化学试卷(解析版) 题型:选择题
已知某温度下纯水中的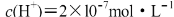 ,对此下列说法正确的是
,对此下列说法正确的是
A.据此无法求算水中c(OH-)
B.该温度低于25℃
C.此温度下水的离子积为常温下的两倍
D.若向水中加入少量盐酸,则水的电离度减小
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省烟台市高三下学期一模诊断测试理科综合化学试卷(解析版) 题型:推断题
(12分)【化学—有机化学基础】
解热镇痛药贝诺酯的合成路线如下:

请回答下列问题:
(1)A→B的反应类型为_____________;B→E的另一产物是________。
(2)X是水杨酸的同分异构体,X中含有苯环,属于酯类,遇FeCl3溶液显紫色。则X 的结构简式为_____________(任写一种)。
(3)F中官能团的名称为________________。1mol扑热息痛与足量NaOH溶液反应,消耗NaOH的物质的量为__________。
(4)生成贝诺酯的化学方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省烟台市高三下学期一模诊断测试理科综合化学试卷(解析版) 题型:选择题
一定温度压强下,在容积可变的密闭容器中发生反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,则下列说法不正确的是
CO2(g)+H2(g) ΔH<0,则下列说法不正确的是
A.其他条件不变,加催化剂与不加催化剂其ΔH 相同
B.当达到平衡,向体系中充入CO2其平衡向左移动
C.理论上该反应可设计成燃料电池,H2O(g)在正极上发生还原反应
D.平衡混合气体通入NaOH溶液恰好反应,升高温度溶液碱性增强,其pH一定增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省泰安市高三下学期一模理科综合化学试卷(解析版) 题型:填空题
铁、铝及其化合物的应用十分广泛,请回答:
(1)在实验室中,硝酸铝必须与可燃物分开存放,是因为硝酸铝具有____________(填字母序号)。
A.可燃性 B.氧化性 C.还原性
(2)已知:当Al(NO3),溶液中pH>3时,铝元素有多种存在形态,如A13+、[Al(OH)]2+、[Al(OH)2]+等,各形态之间可相互转化,写出该溶液中[Al(OH)]2+转化为[Al(OH)2]+的离子方程式_________________。
(3)氯化铁溶液常用作印刷电路铜板的腐蚀剂,反应的离子方程式为___________;从腐蚀废液中回收金属铜还需要的试剂是__________。
(4)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160 mL5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L氢气(标准状况),溶液中铁元素的存在形式为________(填离子符号),检验该离子的实验操作、现象和结论是_________;参加反应的铁粉的质量为______________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省稳派教育高三一轮复习质量检测理科综合化学试卷(解析版) 题型:选择题
下列实验中,现象和离子方程式正确的是
操作 | 现象 | 离子方程式 | |
A | 用CH3COOH溶液浸泡水垢 | 水垢溶解,有无色气泡 | CaCO3+2H+=Ca2++H2O+CO2↑ |
B | 向NaAlO2溶液中通入过量CO2 | 产生白色沉淀 | 2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
C | 向FeBr2溶液中通入过量Cl2 | 溶液由浅绿色变成黄色 | Cl2+2Fe2+ =2Cl- +2Fe3+ |
D | 用石墨电极电解滴有酚酞的饱和NaCl溶液 | 在两极有气体产生,阴 极附近溶液呈现红色 | 2Cl-+2H2O |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省六校高三3月联考化学试卷(解析版) 题型:填空题
选考[化学—选修化学与技术](15分)
通常情况下,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,各国都在限制CO2的排量,同时也加强对CO2创新利用的研究。
(1)目前,推广用超临界CO2(介于气态和液态之间)代替氟利昂作致冷剂,这一做法对环境的积极意义是 。
(2)科学家为提取空气中的CO2,把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应使之变为可再生燃料甲醇。流程如图:
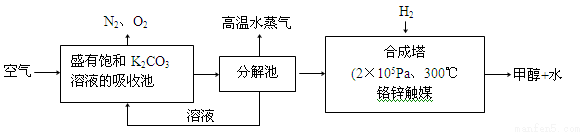
①分解池中反应的化学方程式为: 。
②合成塔中,若有4.4g CO2与足量H2恰好反应生成气态产物,放出4.947kJ的热量,写出该反应的热化学方程式: 。
(3)某同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积Ksp分别为4.96×10-9、2.58×10-9。他最好将空气通入足量的 溶液,实验时除测定温度、压强和空气的体积外,还需测定 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com