
将铁屑溶于过量的稀盐酸后,再加入下列物质,会有Fe3+生成的是 ( )。
A.硫酸 B.氯水
C.硫酸锌 D.氯化铜
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
铁镍蓄电池,放电时的总反应为Fe+Ni2O3+3H2O==Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是
A.电池的电解液为碱性溶液,负极为Fe
B.电池放电过程中,正极附近溶液的pH增大
C.电池放电时,电解质溶液中OH-移向正极
D.电池放电时,负极反应为Fe+2OH--2e-==Fe(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
硅及其化合物在自然界广泛存在并被人类应用。
(1)氮化硅膜与二氧化硅膜相比较具有表面化学性能稳定等优点,故氮化硅膜可用于半导体工业。可以用NH3和SiH4(硅烷)在一定条件下反应,并在600 T的加热基板上生成氮化硅膜:
3SiH4+4NH3 Si3N4+12H2
Si3N4+12H2
以硅化镁为原料制备硅烷的反应和工业流程如下:
反应原理:4NH4Cl+Mg2Si 4NH3↑+SiH4↑+2MgCl2 (ΔH<0)
4NH3↑+SiH4↑+2MgCl2 (ΔH<0)

①NH4Cl中的化学键类型有______________________,SiH4的电子式为______________。
②上述生产硅烷的过程中液氨的作用是____________________ _________________________________________________________。
 ③氨气是重要的工业原料,写出氨气发生催化氧化反应生成NO的化学方程式______________________,
③氨气是重要的工业原料,写出氨气发生催化氧化反应生成NO的化学方程式______________________,
实验室可利用如右图所示装置完成该反应。在实验过程中,除观察到锥形瓶中产生红棕色气体外,还可观察到有白烟生成,白烟的主要成分是______________。
(2)三硅酸镁(Mg2Si3O8·nH2O)难溶于水,在医药上可做抗酸剂。它除了可以中和胃液中多余的酸之外,生成的H2SiO3还可覆盖在有溃疡的胃表面,保护其不再受刺激。三硅酸镁与盐酸反应的化学方程式为__________________ _________________________________________。将0.184 g三硅酸镁加入到50 mL 0.1 mol·L-1盐酸中,充分反应后,滤去沉淀,用0.1 mol·L-1 NaOH溶液滴定剩余的盐酸,消耗NaOH溶液30 mL,则Mg2Si3O8·nH2O中的n值为________。(注:Mg2Si3O8的摩尔质量为260 g·mol-1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某合金与铁的物理性质的比较如下表所示:
| 熔点/℃ | 密度/g·cm-3 | 硬度(金刚石为10) | 导电性(银为100) | |
| 某合金 | 2 500 | 3.00 | 7.4 | 2.3 |
| 铁 | 1 535 | 7.86 | 4.5 | 17 |
还知该合金耐腐蚀,强度大,从以上性能看,该合金不适合作 ( )。
A.导线 B.门窗框
C.炉具 D.飞机外壳
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上以废铜为原料经一系列化学反应可生产氯化亚铜(CuCl),其工艺流程如下图所示:
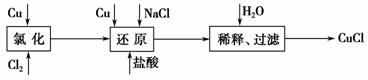
试回答下列问题:
(1)工业生产Cl2时,尾气常用石灰乳吸收,而不用烧碱溶液吸收的原因是______________________________________________________________。
(2)还原过程中的产物为Na[CuCl2],试写出反应的化学方程式___________ ____________________________________________________________。
制备过程中当氯化完成后必须经还原过程再制得CuCl,为什么不用一步法制得CuCl?
(已知Cu2++Cu+2Cl-===2CuCl)
___________________________________________________________。
(3)还原过程中加入少量盐酸的作用是________________________,加入过量NaCl的原因是___________________________________________________ ___________________________________________________。
(4)合成结束后所得产品用酒精淋洗的目的是___________________________ ___________________________________________________。
(5)实验室中在CuCl2热溶液中通入SO2气体也可制备白色的CuCl沉淀,试写出该反应的离子方程式________________________________________ ______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向某晶体的溶液中加入含Fe2+的溶液无明显变化,当滴加几滴溴水后,混合液出现红色,由此得出下列的结论错误的是 ( )。
A.Fe3+的氧化性比溴的氧化性强
B.该晶体中一定含有SCN-
C.Fe2+与SCN-不能形成红色化合物
D.Fe2+被溴氧化成Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量的镁和铝均匀混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是 ( )。
A.3 mol·L-1盐酸 B.4 mol·L-1 HNO3溶液
C.5 mol·L-1 NaOH溶液 D.18.4 mol·L-1 H2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
某干燥粉末可能由Na2O、Na2O2、Na2CO3、NaHCO3、NaCl中的一种或几种组成。将该粉末与足量的盐酸反应有气体X逸出,X通过足量的NaOH溶液后体积缩小(同温同压下测定)。若将该粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原粉末的质量。下列判断正确的是 ( )。
A.粉末中一定有Na2O、Na2O2、NaHCO3
B.粉末中一定不含有Na2CO3和NaCl
C.粉末中一定不含有Na2O和NaCl
D.无法肯定粉末里是否含有NaHCO3和NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分类标准和分类结果不科学的是
| 选项 | 分类目标 | 分类标准 | 分类结果 |
| A | 化学反应 | 有无离子参加或生成 | 离子反应和非离子反应 |
| B | 有无单质参加或生成 | 氧化还原反应和非氧化还原反应 | |
| C | 化学物质 | 分散质粒子大小 | 胶体、溶液和浊液 |
| D | 化合物在水溶液或熔融状态下能否导电 | 电解质和非电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com