
某校研究学习小组同学在实验时把SO2通入装有1mol/LBaCl2溶液的试管中,出现了白色浑浊物。
(1)实验小组的同学根据沉淀溶解平衡原理查阅了工具书上的相关数据,经过计算推导得出:常温下即使把SO2通入1mol/L BaCl2溶液中至饱和,也不可能生成BaSO3沉淀,故白色浑浊物只能是BaSO4。你认为所查阅的数据为: 。
(2)二氧化硫通入氯化钡溶液中理论上不产生沉淀,而实际受到空气和溶液中氧气的影响很快便能观察到沉淀现象.为了避免产生沉淀,某化学小组设计了如下实验装置,实验操作步骤如下:

①气密性检查完好后,在装置A中的多孔隔板上放上锌粒,通过 全【品教学网, 用后离不了!注入稀硫酸.打开活塞,将产生的氢气导入到后续装置.
②D中气泡均匀冒出并验纯全【品教学网, 用后离不了!后关闭活塞,将装置D的导管插入烧杯中。
③通过装置B的 全【品教学网, 用后离不了!滴加浓硫酸,产生的气体进入到BaCl2溶液中,溶液保持澄清。
④打开活塞,将产生的氢气导入后续装置一段时间。
⑤将盛有BaCl2溶液的试管从装置中取出,拔去橡皮塞用胶头滴管伸入到苯层下方滴加双氧水,随即出现白色浑浊,滴加稀盐酸并振荡,白色浑浊不消失。
⑥拆卸装置,清洗仪器,处理剩余药品。
请回答下列问题
(2)实验步骤①和③的空白处使用的仪器名称分别为 、 全【品教学网, 用后离不了!;
(3)反应开始前,先向制取SO2的装置中通入纯净的A中产生的氢气,其作用是: 。
(4)装置C中苯的作用是 。
(5)装置D的目的是 全【品教学网, 用后离不了!
(6)写出实验步骤⑤试管中发生反应的化学方程式 、 全【品教学网, 用后离不了!;
【知识点】二氧化硫的制备、性质及实验探究
【答案解析】(16分)(1)SO2饱和溶液中各离子的浓度、(SO2的溶解度、亚硫酸的电离平衡常数)以及 BaSO3的溶度积常数(BaSO3的溶解度或Ksp(BaSO3)全【品教学网, 用后离不了!)。(2分)(2)长颈漏斗全【品教学网, 用后离不了!、 分液漏斗(2分)(3)赶出装置中的空气防止H2SO3被氧化(2分)(4)将BaCl2溶液与空气隔离,防止H2SO3被氧化全【品教学网, 用后离不了!;(2分)(5)除去SO2防止污染空气(2分)(6)SO2+H2O2=H2SO4、(或H2SO3+H2O2=H2SO4+H2O) H2SO4+BaCl2=BaSO4↓+2HCl全【品教学网, 用后离不了!;(4分)
解析:(1)能够生成BaSO3沉淀,需要查阅SO2饱和溶液中各离子的浓度。(2)可以通过长颈漏斗实现锌粒和酸的接触,分液漏斗的结构和长颈漏斗有很大异,分液漏斗有盖有旋塞,长颈漏斗都没有。(3)A装置获取氢气的作用是赶出装置中的气体,防止二氧化硫通入氯化钡溶液后的现象受到空气和溶液中氧气的影响。(4)苯密度比水小,在氯化钡溶液的上层,可以起到隔离空气的作用。(5)二氧化硫有毒,为了防止造成污染,在实验结束时要再次打开活塞,将产生的氢气导入后续装置一段时间,让SO2全部被氢氧化钠吸收以防止污染。(6)双氧水具有氧化性,可以将二氧化硫氧化为硫酸,进而和氯化钡反应生成沉淀,发生的化学反应为:SO2+H2O2=H2SO4、H2SO4+BaCl2=BaSO4↓+2HCl。
【思路点拨】本题综合考查二氧化硫的制备、性质及实验探究,具有一定的综合性,能够比较全面考查考生基础知识和基本技能。难度较大,区分度较好。


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
H2O2是一种绿色氧化还原试剂,在化学研究中应用广泛。
(1)某小组拟在同浓度Fe3+的催化下,探究H2O2浓度对H2O2分解反应速率的影响。限选试剂与仪器:30% H2O2、0.1mol∙L-1Fe2(SO4)3、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器
①写出本实验H2O2分解反应方程式并标明电子转移的方向和数目:_ ___________
___________
 ②设计实验方案:在不同H2O2浓度下,测定 ________________________
②设计实验方案:在不同H2O2浓度下,测定 ________________________ ____________(要求所测得的数据能直接体现反应速率大
____________(要求所测得的数据能直接体现反应速率大 小)。
小)。
③设计实验装置,完成图20的装置示意图。
④参照下表格式,拟定实验表格,完整体现实验方案(列出所选试剂体积、需记录的待测物理量和所拟定的 数据;数据用字母表示)。
数据;数据用字母表示)。
| 物理量 实验序号 | V[0.1mol·L-1Fe2(SO4)3]/mL | …… | |
| 1 | a | …… | |
| 2 | a | …… |
(2)利用图21(a)和21(b)中的信息,按图21(c)装置(连能的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的_________(填“深”或“浅”),其原因是______________________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量的锌与100mL 18.5mol•L﹣1浓硫酸充分反应后,锌完全溶解,同时生成气体A 33.6L(标准状况).将反应后的溶液稀释至1L,则得溶液中c(H+)=0.1mol•L﹣1,则下列叙述中错误的是( )
|
| A. | 气体A为SO2和H2的混合物 | B. | 气体A中SO2和H2的体积比为1:5 |
|
| C. | 反应中消耗的Zn的质量为97.5 g | D. | 反应中共转移电子3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容密闭容器中发生反应2NO2  2NO+O2,下列所述可以说明反应达到平衡状态的是
2NO+O2,下列所述可以说明反应达到平衡状态的是
①单位时间内生成n molO2的同时生成2n molNO2
②单位时间内生成n molO2的同时生成2n molNO
③混合气体的颜色不再改变
④混合气体的密度不再改变
A.①③ B.②④ C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
利用催化氧化反应将SO2转化为SO3是工业上生产
硫酸的关键步骤.
(1)T1℃时,在1L密闭容器中充入0.6molSO3,图1表示SO3
物质的量随时间的变化曲线。
①平衡时,SO3的转化率为 (保留小数点后一位) ;
T1℃时,反应2SO2(g)+O2(g)  2SO3(g) 的平衡常数为 ;其他条件不变,在8min时压缩容器体积至0.5L,则n(SO3
2SO3(g) 的平衡常数为 ;其他条件不变,在8min时压缩容器体积至0.5L,则n(SO3 )的变化曲线为 (填字母)。
)的变化曲线为 (填字母)。
②下表为不同温度(T)下,反应2SO2(g)+O2(g)  2SO3(g) (△H<0)的化学平衡常数(K)
2SO3(g) (△H<0)的化学平衡常数(K)
| T/℃ | T2 | T3 |
| K | 20.5 | 4.68 |
由此推知,温度最低的是 (填“T1”、“T2” 或 “T3”)。
③在温度为T1℃时,向该1L的密闭容器中同时加入0.2molSO2、xmolO2、0.2molSO3三种气体,在达到平衡前若要使SO3的浓度减小,则x的取值范围是 。
(2)科学家研究出用电化学原理生产硫酸的新工艺,装置如图2所示,总反应的化学方程式为 ,其阳极的电极反应式为
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生用量筒量取液体,初
次视线与量筒内凹液面的最低处保持水平,读数为9.8mL。倒出部分液体后,俯视凹液面的最低处,读数为3.5mL,则该学生实际倒出液体的体积
A.大于6.3mL B.小于6.3mL C.等于6.3mL D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2、NO是大气污染物。吸收SO2 和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

(1)装置Ⅰ中生成HSO3-的离子方程为 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如右图所示。

①下列说法正确的是 (填字母序号)。
a.pH=8时,溶液中c(HSO3-) < c(SO32-)
b.pH=7时,溶液中c(Na+) =c(HSO3-)+c(SO32-)
c.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
(3)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式 。
(4)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示。
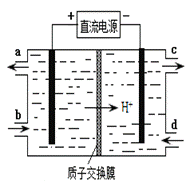
①生成Ce4+的电极反应式为 。
②生成Ce4+从电解槽的 (填字母序号)口流出。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g·L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作不正确的是
A.吸滤完毕停止吸滤时,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关闭水龙头全【品教学网, 用后离不了!
B.分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
查看答案和解析>>
科目:高中化学 来源: 题型:
香豆素是一种天然香料,存在于黑香豆、兰花等植物中。工业上常用水杨醛与乙酸酐在催化剂存在
下加热反应制得:
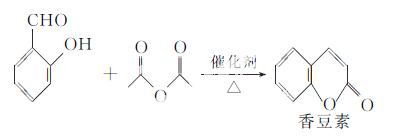
以下是由甲苯为原料生产香豆素的一种合成路线(部分反应条件及副产物已略去):
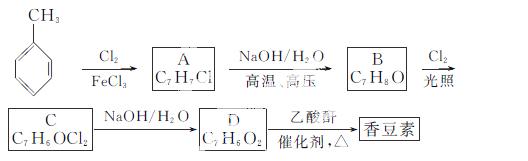
已知以下信息:
①A中有五种不同化学环境的氢;
②B可与FeCl3溶液发生显色反应;
③同一个碳原子上连有两个羟基通常不稳定,易脱水形成羰基。
请回答下列问题:
(1)香豆素的分子式为__________;
(2)由甲苯生成A的反应类型为__________,A的化学名称为__________;
(3)由B生成C的化学反应方程式为__________________________________;
(4)B的同分异构体中含有苯环的还有__________种,其中在核磁共振氢谱中只出现四组峰的有________种;
(5)D的同分异构体中含有苯环的还有________种,其中:
①既能发生银镜反应,又能发生水解反应的是__________(写结构简式);
②能够与饱和碳酸氢钠溶液反应放出CO2的是__________(写结构简式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com