
| ||

| ||
| c4(H2) |
| c4(H2O) |
| c4(H2) |
| c4(H2O) |


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
A、C+O2
| ||||
| B、Zn+H2SO4═ZnSO4+H2↑ | ||||
C、CaCO3
| ||||
| D、NaCl+AgNO3═NaNO3+AgCl↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
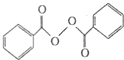 )过去常被用来做面粉增白剂,但目前已被禁用.
)过去常被用来做面粉增白剂,但目前已被禁用.
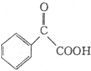 的流程.示例如下:
的流程.示例如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| A、氧化性(酸性溶液):PbO2>Fe3+>S |
| B、还原性(碱性溶液):Fe(OH)2>KCl>Cl2 |
| C、酸性(水溶液):H2S>H2SO4>H2SeO4>HN3 |
| D、热稳定性:BaCO3>MgCO3>CuCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④⑤ | B、①④ | C、②③⑤ | D、②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1 (NH4)2Fe(SO4)2溶液:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) |
| B、0.1 mol?L-1 NaHCO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| C、0.1 mol?L-1Na2S溶液:2c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| D、0.01 mol?L-1NaOH溶液与等体积pH=2的醋酸混合后的溶液:c (CH3COO-)>c (Na+)>c (H+)>c (OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间(min) 浓度(mol.L-1) 实验序号/温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 |
| 实验1/800 | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
| 实验2/800 | 1.00 | 0.70 | 0.50 | 0.50 | 0.50 | 0.50 |
| 实验3/800 | 1.00 | 0.50 | 0.40 | 0.15 | 0.15 | 0.15 |
| A、实验2比实验1的反应容器内压强减小 |
| B、实验2比实验l使用了效率更高的催化剂 |
| C、实验1比实验3的平衡常数大 |
| D、实验2和实验3可判断该反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、遇苯酚变紫色的溶液:Na+、Mg2+、SO42-、Cl- |
| B、0.1 mol?L-1 (NH4)2Fe(SO4)2溶液中:K+、Cu2+、Cl-、MnO4- |
| C、使甲基橙变红色的溶液:NH4+、Cu2+、ClO-、Cl- |
| D、0.1mol?L-1 NaHCO3溶液:K+、AlO2-、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com