

 CaS+Na2CO3+2CO2↑
CaS+Na2CO3+2CO2↑ CaS+Na2CO3+2CO2↑。
CaS+Na2CO3+2CO2↑。

科目:高中化学 来源:不详 题型:单选题
| A.MgO、Al2O3的熔点很高,可制作耐高温材料 |
| B.NaHCO3能与碱反应,食品工业上用作焙制糕点的膨松剂 |
| C.Al具有良好的延展性和抗腐蚀性,可制成铝箔包装物品 |
| D.利用钠蒸气放电发光的性质制造的高压钠灯,可发出射程远、透雾能力强的黄光 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.有气体生成 |
| B.钠熔化成小球并在液面上游动 |
| C.烧杯底部有银白色的金属钙生成 |
| D.溶液变浑浊 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
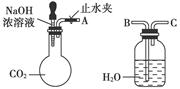
| A.NaOH和Na2CO3; | |
| B.; | |
| C.; | D.。 |
| 实验操作 | 实验现象 | 结论 |
| (1)取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | | |
| (2) | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| A.加水,将湿润的红色石蕊试纸放在试管口 |
| B.加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口 |
| C.加氢氧化钠溶液,加热,滴入酚酞试剂 |
| D.加氢氧化钠溶液,加热,滴入紫色石蕊试剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| 实验操作 | 实验现象 | 结论 |
| ①取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | | |
| ② | | |

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
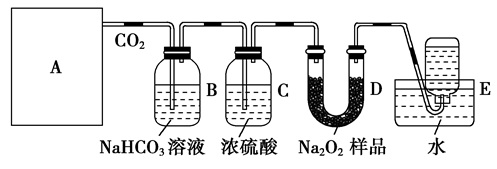
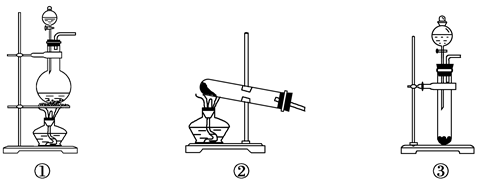
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com