
 用如图所示装置进行中和热测定实验,请回答下列问题:
用如图所示装置进行中和热测定实验,请回答下列问题:

 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
| A、a=b=c |
| B、a=c>b |
| C、b>a>c |
| D、c>a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,芳香烃A能发生如图一系列转化:
,芳香烃A能发生如图一系列转化:
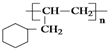 的线路.(用A→…→目标产物 在箭号上写明反应试剂及反应条件.)
的线路.(用A→…→目标产物 在箭号上写明反应试剂及反应条件.)查看答案和解析>>
科目:高中化学 来源: 题型:
| 14 |
| 6 |
| 14 |
| 7 |
| 16 |
| 8 |
| 35 |
| 17 |
| 235 |
| 92 |
| 238 |
| 92 |
查看答案和解析>>
科目:高中化学 来源: 题型:
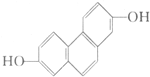 质子核磁共振谱是研究有机化合物结构的有力手段之一.结构中的等效氢原子核磁共振谱中都给出了相应的峰值 (信号),谱中峰的强度与结构中的H原子数成正比.试回答,结构简式为如图所示的有机化合物:
质子核磁共振谱是研究有机化合物结构的有力手段之一.结构中的等效氢原子核磁共振谱中都给出了相应的峰值 (信号),谱中峰的强度与结构中的H原子数成正比.试回答,结构简式为如图所示的有机化合物:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含0.2mol H2SO4的浓硫酸与足量锌反应,生成气体的分子数小于0.1NA |
| B、标况下,22.4L四氯化碳所含分子数大于NA |
| C、0.1mol/L的AgNO3溶液中,阳离子所带正电荷数目为0.1NA |
| D、0.2mol/L的H2SO4的硫酸溶液与0.1mol/L的H2SO4的硫酸溶液等质量混合溶液浓度大于0.15mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com