
 ��W��X��Y�����Ӱ뾶�ɴ�С��˳��ΪS2-��O2-��Al3+�������ӷ��Żش�
��W��X��Y�����Ӱ뾶�ɴ�С��˳��ΪS2-��O2-��Al3+�������ӷ��Żش����� Q��W��X��Y��Z�����ڱ�ǰ36��Ԫ���е����ֳ���Ԫ�أ���ԭ��������������Wԭ������������������������֮��Ϊ3��4����WΪ��Ԫ�أ�Q��Y���������ǵ����������Ҫ���ʣ���Q��YΪS��NԪ�أ�����ԭ��������������QΪ��Ԫ�أ�YΪ��Ԫ�أ�X�ǵؿ��к�����ߵĽ���Ԫ�أ���X����Ԫ�أ�Z���γɺ�ɫ����ש��ɫ����Z2O�ͺ�ɫ��ZO�����������Z��ͭԪ�أ��ݴ˽���С�⼴�ɣ�
��� �⣺���ݷ�����֪��QΪN��WΪO��XΪAl��YΪS��ZΪCu��
��1��QΪ��Ԫ�أ����������д��ڵ�����������ԭ�������Ϊ8���ӣ�N2�ĵ���ʽΪ�� ��Ԫ�����ӵ��Ӳ���Խ�࣬�뾶Խ��������Ų���ͬ�����ӣ�ԭ������ԽС�����Ӱ뾶Խ��O��Al��S�����Ӱ뾶�ɴ�С��˳��Ϊ��S2-��O2-��Al3+���ʴ�Ϊ��
��Ԫ�����ӵ��Ӳ���Խ�࣬�뾶Խ��������Ų���ͬ�����ӣ�ԭ������ԽС�����Ӱ뾶Խ��O��Al��S�����Ӱ뾶�ɴ�С��˳��Ϊ��S2-��O2-��Al3+���ʴ�Ϊ�� ��S2-��O2-��Al3+��
��S2-��O2-��Al3+��
��2��Al��S��ɵĻ��������ˮ�з���˫ˮ�ⷴӦ����Ӧ�Ļ�ѧ����ʽ�ǣ�Al2S3+6H2O=2Al��OH��3��+3H2S�����ʴ�Ϊ��Al2S3+6H2O=2Al��OH��3��+3H2S����
��3��Na2S��Һ�д���S2-����ˮ�⣬��Һ�ʼ��ԣ�����S2-+H2O?HS-+OH-������Һ������Ũ���ɴ�С��˳��Ϊ��c��Na+����c��S2-����c��OH-����c��HS-����c��H+�����ʴ�Ϊ��c��Na+����c��S2-����c��OH-����c��HS-����c��H+����
��4��CuO�ڸ������백�����ɵ�������Ӧ�Ļ�ѧ����ʽΪ��3CuO+2NH3$\frac{\underline{\;����\;}}{\;}$3Cu+N2+3H2O���ʴ�Ϊ��3CuO+2NH3$\frac{\underline{\;����\;}}{\;}$3Cu+N2+3H2O��
��5��Fe��OH��3��Ksp=10-35����ѧ����Ϊ��������Һ�е�����Ũ��С��1��10-5mol/Lʱ�������ʹ���ȫ���ʴ�ʱ��Һ��c��OH-��=$\root{3}{\frac{1{0}^{-35}}{1{0}^{-5}}}$=10-10���ʴ�ʱc��H+��=$\frac{1{0}^{-14}}{1{0}^{-10}}$=10-4���ʴ�ʱpHֵΪ4����CuCl2��Һ�л���FeCl3����ʱ���ɼ�������ͭ����pHΪ4��Ȼ���ٹ��ˣ��ʴ�Ϊ��CuO��4��
��6����ҵ�Ͽ��ø���������Cu2S+O2�T2Cu+SO2��ұ������Cu����Ӧ��Cu�Ļ��ϼ���+1�۱�Ϊ0�ۣ�2molCuԪ��ת��2mol���ӣ�OԪ����0�۱�Ϊ-2�ۣ�1mol����ת��4mol���ӣ�������2molCuʱת�Ƶ�����Ϊ6mol������1molCuת��3mol���ӣ��ʴ�Ϊ��3��
���� �����Ƕ����ʽṹ�Ŀ��飬�ƶ�Ԫ���ǽ���ؼ����漰����ʽ�����Ӱ뾶��С�Ƚϡ�����Ũ�ȴ�С�Ƚϡ�������ԭ��Ӧ�ȣ���Ҫѧ���߱���ʵ�Ļ���֪ʶ���Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A��ʳ�ü����Ҫ�ɷ�Ϊ�������� | B�����˵���Ҫ�ɷ�Ϊ����� | C��ͭ�̵���Ҫ�ɷ�Ϊ������ͭ | D��Ư��Һ����Ч�ɷ�Ϊ�������� |
 |  |  |  |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
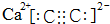 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Һ�еμӹ�����ˮ��Ag++NH3•H2O=AgOH��+NH4+ | |
| B�� | NaHS��Һ�ʼ��ԣ�HS-+H3O+?H2S+H2O | |
| C�� | 4 mol•L-1��KAl��SO4��2��Һ��7 mol•L-1��Ba��OH��2��Һ�������ϣ�4Al3++7SO42-+7Ba2++14OH-=2Al��OH��3��+2AlO2-+7BaSO4��+4H2O | |
| D�� | ʳ�������ˮƿ��ˮ����2H++CaCO3=Ca2++H2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
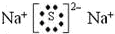 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ���Ӱ뾶��W3+��Z+��Y2- | |
| B�� | X��Y������ͬ���������� | |
| C�� | Z��Y�γɵĻ�������ֻ�������Ӽ� | |
| D�� | �����µ���W������R������������Ӧˮ�����Ũ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
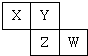
| A�� | Ԫ��X����Ȼ�����γɻ�������������Ԫ�� | |
| B�� | ��̬�⻯����ȶ���Z��W��Y | |
| C�� | ԭ�Ӱ뾶�ɴ�С����˳��Z��Y��X | |
| D�� | Wֻ��һ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 b��
b��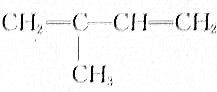
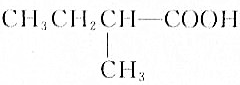 f��HOOC��CH2��4COOH
f��HOOC��CH2��4COOH ��
��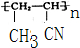
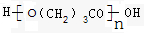
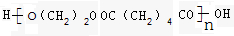 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com