
 ,可用作抗凝血药.下列关于双香豆素的推论中错误的是( )
,可用作抗凝血药.下列关于双香豆素的推论中错误的是( )| A. | 分子式为C19H14O6,能与NaOH溶液反应 | |
| B. | 食草动物食用腐败草料后,在受外伤时血液不容易凝固 | |
| C. | 分子中所有碳原子不可能在同一平面 | |
| D. | 可发生水解、加成、氧化、还原反应 |
分析 由双香豆素的结构可知,分子中含-COOC-、-OH、碳碳双键,结合酯、醇、烯烃的性质来解答.
解答 解:A.双香豆素的分子式为C19H12O6,故A错误;
B.为抗凝血药,则受外伤时血液不容易凝固,故B正确;
C.根据苯分子结构中6个碳原子共平面,以及乙烯分子中6原子共平面,判断知该分子中所有碳原子有可能在同一平面,故C错误;
D.含有酯基,可发生水解反应,含有苯环,可发生加成反应、还原反应,含有酚羟基,可发生氧化反应,故D正确.
故选AC.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意常见有机物的官能团的性质,为解答该类题目的关键,难度不大.


科目:高中化学 来源: 题型:解答题
 光伏产业作为我国战略性新兴产业之一,多晶硅是重要原料.
光伏产业作为我国战略性新兴产业之一,多晶硅是重要原料.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | c(CO)=c(H2) | |
| B. | 单位时间内断裂2个H-O键的同时生成了1个H-H键 | |
| C. | 容器内反应温度不再改变 | |
| D. | 容器内的混合气体密度保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
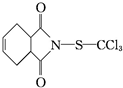 )是一种广谱性的主要用于叶面保护的杀菌剂,无药害,在果树、蔬菜及各种经济作物上使用.下列说法正确的是( )
)是一种广谱性的主要用于叶面保护的杀菌剂,无药害,在果树、蔬菜及各种经济作物上使用.下列说法正确的是( )| A. | 克菌丹的分子式为C9H8O2NSCl3,属于芳香族化合物 | |
| B. | 克菌丹易溶于水,在加热条件下不能与NaOH溶液反应 | |
| C. | 克菌丹能与溴的CCl4溶液发生取代反应使之褪色 | |
| D. | 克菌丹在一定条件下能发生取代、加聚等反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe | B. | MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑ | ||
| C. | 2AlCl3$\frac{\underline{\;通电\;}}{\;}$2Al+3Cl2↑ | D. | 2Ag2O$\frac{\underline{\;\;△\;\;}}{\;}$4Ag+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液中MgCl2的物质的量为0.1 mol | |
| B. | 当加入87.5 mL NaOH溶液时,沉淀质量最大 | |
| C. | 当加入90.0 mL NaOH溶液时,溶液中NaAlO2与NaCl的物质的量之比为2:35 | |
| D. | 当100 mL NaOH溶液刚好完全消耗时,Al3+恰好全部转化为Al${O}_{2}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com