
【题目】下列说法正确的是( )
A.乙酸是一种弱酸,不能和碳酸钙反应放出二氧化碳气体
B.润滑油属于酯类
C.没有成熟的苹果汁遇碘变蓝色,成熟的苹果汁能还原新制氢氧化铜悬浊液
D.糖类、油脂、蛋白质都是由C,H,O三种元素组成
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)水被称为“生命之源”,为了给某地区的人民寻找合适的饮用水源,某化学小组对附近山上的泉水进行了分析,结果显示水体硬度超标,其水体中主要含Ca2+、Mg2+、HCO3﹣和Cl﹣ . 则该水源属于(填“暂时”或“永久”)硬水,可通过加热煮沸来降低水体的硬度,水体中的Ca2+、Mg2+在加热煮沸后将分别转化为、形成水垢.
(2)我国化工专家侯德榜,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献.生产流程如图: 
①向沉淀池中通入NH3和CO2气体时,正确的顺序是 .
②流程图中X表示的物质是
(3)贵州铝厂是目前我国最大的电解铝生产基地.所需生产原料Al2O3可以从铝土矿(主要成分是Al2O3 , 含SiO2、Fe2O3、MgO等杂质)中提取,其工艺流程如下: 
请回答下列问题:
①固体A是 , 滤液E中含有的溶质是
②已知298K时,Mg(OH)2的容度积常数Ksp=5.6×10﹣12 , 取适量的滤液B,加入一定量的烧碱达到沉淀溶解平衡时,测得pH=13.0,则此时溶液中的c(Mg2+)=molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在强碱性溶液中一定能大量共存的是( )
A. Na+、NH4+、SO42-B. Ag+、Fe3+、Cl-
C. Ba2+、K+、NO3-D. K+、Ba2+、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

请填写下列空白:
(1)步骤①灼烧海带的目的是_____,除需要三脚架、玻璃棒、酒精灯之 外还需要用到的实验仪器是_________;
(2)步骤③实验操作名称是_____,步骤⑤用到的玻璃仪器是_____;
(3)如何检验步骤③后得到溶液中是否含有 I-________________;
(4)步骤④反应的离子方程式是_____;
(5)步骤④通入的氯气不能过量,理由是_____;
(6)步骤⑤中,某学生选择用苯来提取碘的理由是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合利用CO2、CO对构建低碳社会有重要意义.
(1)固体氧化物电解池(SOEC)用于高温电解CO2和H2O的混合气体,既可高效制备合成气(CO+H2),又可实现CO2的减排,其工作原理如图.
①b为电源的(填“正极”或“负极”)
②写出电极c发生的电极反应式、 .
(2)电解生成的合成气在催化剂作用下发生如下反应:CO(g)+2H2(g)CH3OH(g).对此反应进行如下研究:某温度下在一恒压容器中分别充入1.2mol CO和1mol H2 , 达到平衡时容器体积为2L,且含有0.4mol CH3OH(g),则该反应平衡常数值为 , 此时向容器中再通入0.35molCO气体,则此平衡将移动(填“向正反应方向”、“不”或“逆反应方向”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组用如图1装置进行实验,试回答下列问题. 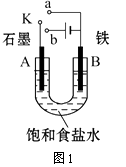
(1)若开始时开关K与a连接,则B极的电极反应式为 .
(2)若开始时开关K与b连接,则B极的电极反应式为 , 总反应的离子方程式为 . 有关上述实验,下列说法正确的是(填序号) .
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24L气体,则溶液中转移0.2mol电子
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图2装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾. 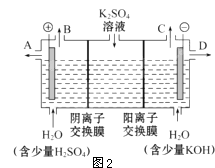
①该电解槽的阳极反应式为 .
此时通过阴离子交换膜的离子数(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数.
②若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的比较,错误的是( )
A.溶解度(25℃):小苏打 < 苏打B.沸点:H2Se>H2S>H2O
C.密度:溴乙烷 > 水D.碳碳键键长:乙烯 < 苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表:
化合物 | 相对分 | 密度 | 沸点/℃ | 溶解度 |
正丁醇 | 74 | 0.80 | 118.0 | 9 |
冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
操作如下:
①在50mL圆底烧瓶中,加入18.5mL正丁醇和13.4mL冰醋酸,3~4滴浓硫酸,投入沸石.安装分水器(作用:实验过程中不断分离除去反应生成的水)及回流冷凝管.
②将分水器分出的酯层和反应液一起倒入分液漏斗中,水洗,10% Na2CO3洗涤,再水洗,最后转移至锥形瓶,干燥.
③将干燥后的乙酸正丁酯滤入烧瓶中,常压蒸馏,收集馏分,得15.1g乙酸正丁酯.
请回答有关问题:
(1)冷水应该从冷凝管(填“a”或“b”)端管口通入.
(2)进行分液操作时,使用的漏斗是(填选项).
(3)仪器A中乙酸和正丁醇制备乙酸正丁酯的化学方程为 .
(4)步骤①“不断分离除去反应生成的水”的目的是 .
(5)步骤②中用10% Na2CO3溶液洗涤有机层,该步操作的目的是
(6)乙酸正丁酯的产率为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com