
Na2CO3固体中可能含有杂质K2CO3、NaHCO3、NaCl中一种或几种,取10.6g样品,加入足量的稀盐酸产生气体4.8g,下列分析正确的是()
| A. | 一定含有NaHCO3 | B. | 一定含有K2CO3 | |
| C. | 一定不含NaCl | D. | 一定含有NaCl |
| 几组未知物的检验. | |
| 专题: | 物质检验鉴别题. |
| 分析: | 碳酸钠、碳酸氢钠、碳酸钾分别与稀盐酸反应产生二氧化碳质量进行比较,利用极值对比生成二氧化碳的多少进行分析判断,可以得出本题的答案. |
| 解答: | 解:由Na2CO3+2HCl=2NaCl+H2O+CO2↑、NaHCO3+HCl=NaCl+H2O+CO2↑可知1mol碳酸钠与1mol碳酸氢钠分别与稀盐酸反应,都生成1mol二氧化碳. 碳酸钠的相对分子质量为 由于10.6g碳酸钠与足量的稀盐酸反应生成二氧化碳的质量为4.4g,小于10.6g含杂质的碳酸钠与足量的稀盐酸反应生成二氧化碳的质量4.8g.说明所含杂质不能只含氯化钠,因为只含氯化钠时,生成二氧化碳的质量就会小于4.4g;所含杂质只含碳酸氢钠时,生成二氧化碳的质量就会大于4.4g,符合题意;所含杂质只有K2CO3时,生成二氧化碳小于4.4g,所以不符合题意;综上所述样品中一定含有NaHCO3,可能是K2CO3、NaHCO3;或K2CO3、NaHCO3、NaCl;或NaHCO3、NaCl三种组合符合; 故答案为一定含有NaHCO3; 故选A. |
| 点评: | 本题考查有关化学方程式的计算和含杂质物质的推断,主要是利用极值法进行对比分析解决问题,难度较大. |


科目:高中化学 来源: 题型:
在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )
正极附近的SO浓度逐渐增大 B.电子通过导线由铜片流向锌片
C.正极有O2逸出 D.铜片上有H2逸出
查看答案和解析>>
科目:高中化学 来源: 题型:
在同一温度下,当弱电解质溶液a,强电解质溶液b,金属导体c的导电能力相同,若同时升高到相同温度,则它们的导电能力是 ( )
A. a>b>c B. a=b=c C. c>a>b D. b>c>a
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备BaCl2的工艺流程图如下:
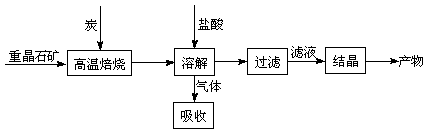
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaS O4(s) + 4C(s)
O4(s) + 4C(s) 4CO(g) + BaS(s) △H1 = 571.2 kJ·mol-1 ①
4CO(g) + BaS(s) △H1 = 571.2 kJ·mol-1 ①
BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
⑴气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
⑵向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,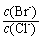 = 。
= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
⑶反应C(s) + CO2(g) 2CO(g)的△H2= kJ·mol-1。
2CO(g)的△H2= kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知水和苯互不相溶,苯不与钠反应,在烧杯中加水和苯(密度:0.88g/cm3)各50mL.将一小粒金属钠(密度:0.97g/cm3)投入烧杯中,观察到的现象可能是()
| A. | 钠在水层中反应并四处游动 | |
| B. | 钠停留在苯层中不发生反应 | |
| C. | 钠在苯的液面上反应并四处游动 | |
| D. | 钠在苯与水的界面处反应并可能做上、下跳动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,调节反应物用量或浓度,或改变反应的温度,不会改变反应产物的是()
①Na与氧气反应②乙醇和浓硫酸共热③二氧化硫通入烧碱溶液 ④硫酸中加入铁粉⑤氨水加入硝酸银溶液 ⑥铁与硝酸溶液 ⑦硫化氢在氧气中燃烧⑧金属钠投入水中.
| A. | ②④⑤ | B. | ①③⑥ | C. | ④⑦ | D. | ⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如右下图所示的装置制取乙酸乙酯,请回答下列问题。
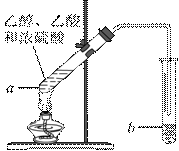 (1)乙醇分子中官能团的名称是________________。
(1)乙醇分子中官能团的名称是________________。
(2)试管a中加入几块碎瓷片的目的是_________。
(3)试管a中发生反应的化学方程式为
___________________________________________,
反应类型是____________________。
(4)反应开始前,试管b中盛放的溶液是____________。
(5)可用____________的方法把制得的乙酸乙酯分离出来。
查看答案和解析>>
科目:高中化学 来源: 题型:
新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。工业上制备K2FeO4的常用方法有两种。
方法Ⅰ:次氯酸盐氧化法。工艺流程如下图所示。
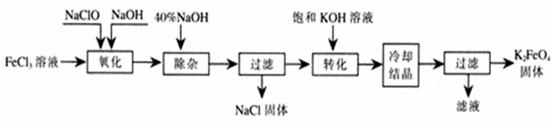
⑴ 写出“氧化”过程中反应的化学方程式: 。
⑵写出“转化”过程中发生反应的化学方程式为 。
⑶上述工艺得到的高铁酸钾常含有杂质,可用重结晶发提纯,操作是:将粗产品用 溶解,然后 。
方法Ⅱ:电解法。以铁为阳极电解氢氧化钠溶液,然后在阳极溶液中加入KOH。
⑷电解时阳极发生反应生成FeO42-,该电极反应方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com