
B、C、N是几种常见的非金属元素,其形成的各种化合物在自然界中广泛存在。
(1)基态硼原子的电子排布式为_________;C、N元素原子的第一电离能由大到小的顺序为_________;
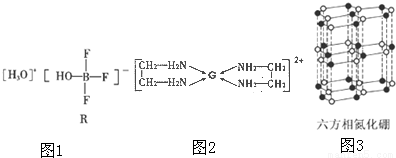
(2)BF3与一定量的水可形成如图1的晶体R。
①晶体R中各种微粒间的作用力涉及_________(填字母);
a.离子键 b.共价键 c.配位键 d.金属键 e.范德华力
②R中阴离子的空间构型为_________;
(3)乙二胺(H2N-CH2-CH2-NH2)与CaCl2溶液可形成配离子(结构如图2)乙二胺分子中氮原子的杂化类型为_________;乙二胺和三甲胺[N(CH3)3]均属于铵,但乙二胺比三甲胺的沸点高得多,原因是__________________;
(4)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,其结构与石墨相似,具有层状结构,可作高温润滑剂;它的晶体结构如图3所示,六方相氮化硼质地软的原因是__________________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
下列关于NH4+、NH3、NH2-三种微粒的说法不正确的是
A.三种微粒所含有的电子数相等
B.三种微粒中氮原子的杂化方式相同
C.三种微粒的空间构型相同
D.键角大小关系:NH4+>NH3>NH2-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省等三校高一下期末化学试卷(解析版) 题型:选择题
已知某主族元素X的原子获得一个电子成为X-离子,则该元素在周期表中所在的族为
①ⅦA族 ②ⅥA族 ③IA族
A. 只可能是①
B. 只可能是③
C. 可能是①或③
D. 可能是①或②或③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二下期末化学试卷(解析版) 题型:实验题
羟基是一种重要的官能团。某化学兴趣小组以①碳酸 ②苯酚 ③乙酸3种物质的溶液作为研究对象,通过实验来比较不同物质的羟基中氢原子的活泼性。
某同学设计并实施了如下实验方案,请完成有关填空。
编号 | 实验操作 | 实验现象 | 结论及解释 |
1 | 分别取3种溶液,滴加紫色石蕊溶液 | 溶液会变红的是①③ | ———————— |
2 | 用足量的乙酸溶液浸泡碳酸钙 | ———————— | 有关反应的化学方程式为__________________ |
3 | 将CO2通入苯酚钠溶液中 | ———————— | 有关反应的离子方程式为__________________ |
结论:3种物质的羟基中的氢原子的活泼性由强到弱的顺序是________(填序号) | |||
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二下期末化学试卷(解析版) 题型:选择题
颠茄酸酯(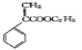 )是一种用于胃肠道平滑肌痉挛及溃疡病的辅助治疗药物,下列说法正确的是
)是一种用于胃肠道平滑肌痉挛及溃疡病的辅助治疗药物,下列说法正确的是
A.不能使酸性KMnO4溶液褪色
B.1mol颠茄酸酯最多与4molBr2发生加成反应
C.能与NaHCO3溶液反应
D.能与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二下期末化学试卷(解析版) 题型:选择题
下列说法中正确的是
A. 电子云通常是用小黑点来表示电子的多少
B. 处于最低能量的原子叫基态原子
C. 能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动
D. 电子仅在激发态跃迁到基态时才会产生原子光谱
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二下期末化学试卷(解析版) 题型:填空题
SOCl2(亚硫酰氯)是一种无色或淡黄色发烟液体,遇水或醇分解成二氧化硫和氯化氢,用途广泛。已知:SO2+Cl2+SCl2=2SOCl2。
(1)SCl2的电子式为_____________________;
(2)上述SOCl2的制备反应中,生成1molSOCl2时转移_______mol电子。
(3)SOCl2与足量NaHCO3溶液反应的离子方程式为_____________________;
(4)无水AlCl3是有机反应的催化剂,也是制备无水四氯铝酸锂(LiAlCl4)的原料,可由AlCl3溶液浓缩结晶得到AlCl3·6H2O,再脱水得到AlCl3。
①若将AlCl3溶液蒸发至干并充分灼烧,则最终得到的固体产物为______________(填化学式)。
②AlCl3·6H2O中加入SOCl2并加热可制得无水氯化铝。SOCl2的作用是________________________________(用文字和方程式说明)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南曲靖一中高一下期末化学试卷(解析版) 题型:选择题
对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述中正确的是( )
4NO(g)+6H2O(g),下列叙述中正确的是( )
A.达到化学平衡时4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达平衡状态
C.达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大
D.平衡混合物中各物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北承德隆化县存瑞中学高一下第一次质检化学试卷(解析版) 题型:选择题
某元素二价阴离子的核外有18个电子,质量数为32,该元素原子的原子核中的中子数为( )
A. 12 B. 14 C. 16 D. 18
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com