
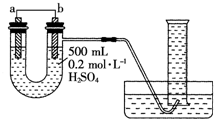
 现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题:
现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题:分析 (1)纯铜片和纯锌片、稀硫酸组成原电池,由图可知b电极处有氢气生成,则b为铜,为正极;a为锌,为负极;b上氢离子得电子生成氢气;
(2)如果将a、b两电极的电极材料对调,则右边为锌失电子作负极,左边为铜为正极,氢离子得电子生成氢气;
(3)根据电极方程式结合气体的物质的量求算电子的物质的量,a极为Zn作负极失电子,根据电子守恒计算Zn的质量.
解答 解:(1)纯铜片和纯锌片、稀硫酸组成原电池,由图可知b电极处有氢气生成,则b为铜,为正极;a为锌,为负极;b上氢离子得电子生成氢气,其电极反应式为:2H++2e-═H2↑,
故答案为:铜;2H++2e-═H2↑;
(2)如果将a、b两电极的电极材料对调,则右边为锌失电子作负极,左边为铜为正极,氢离子得电子生成氢气,则左边上有氢气生成,所以U形管中左端溶夜下降,右端溶夜上升;故答案为:左端溶夜下降,右端溶夜上升;
(3)当量筒中收集到672mL(标准状况下)气体,则n(H2)=$\frac{V}{Vm}$=$\frac{0.672L}{22.4L/mol}$=0.03mol,已知b上的电极反应式为:2H++2e-═H2↑,则通过导线的电子的物质的量为0.06mol,a电极上的反应为:Zn-2e-═Zn2+,则溶解的Zn的物质的量为0.03mol,则减小的Zn的质量为65g/mol×0.03mol=1.95g,
故答案为:0.06;减小;1.95.
点评 本题考查了原电池的工作原理知识,主要考查正负极的判断、电极方程式的书写、电子守恒在计算中的应用等,注意知识的积累是解题关键,难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4mol/L | B. | 1.4mol/L | C. | 1.2mol/L | D. | 0.7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 时间/min | 0 | 20 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.020 | 0.020 | 0.020 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | L | M | Q |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.112 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +7、-1 | +2 | -2 |
| A. | 等物质的量的X、Y的单质与足量盐酸反应,生成H2一样多 | |
| B. | Y与Q形成的化合物不可能跟氢氧化钠溶液反应 | |
| C. | Z的氢化物的稳定性强于L的氢化物的稳定性 | |
| D. | 与稀盐酸反应的剧烈程度:M单质<X单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤⑦ | B. | ②③④⑤⑥ | C. | ③④⑥ | D. | ②③④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y、Z的浓度相等 | B. | X、Y、Z在容器中共存 | ||
| C. | 正、逆反应速率都等于零 | D. | X、Y、Z的浓度均不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配位体是Cl-和H2O,配位数是9 | |
| B. | 中心离子是Ti4+,配离子是[TiCl(H2O)5]2+ | |
| C. | 内界和外界中的Cl-的数目比是1:2 | |
| D. | 加入足量AgNO3溶液,所有Cl-均被完全沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同一化学反应中用各反应物及各生成物表示的速度相等 | |
| B. | 无论何种反应,在其它条件不变的情况下,升温速度则加快 | |
| C. | 无论何种反应改变压强就能改变其速度 | |
| D. | 用单位时间内某物质浓度的改变量所表示的速度是即时速度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com