
【题目】用下列装置进行实验,能达到相应实验目的的是

A. 图甲可用于蒸馏石油并收集60~150℃馏分
B. 图乙可用于除去乙烯气体中混有的少量SO2
C. 图丙装置可用于比较S、C、Si三种元素的非金属性
D. 图丁装置可用于测定CO2的生成速率
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】室温下向10mL0.1mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如闬所示.下列说法正确的是( ) 
A.a 点所示溶液中 c(Na+)>c(A﹣)>c(H+)>c(HA)
B.a、b 两点所示溶液中水的电离程度相问
C.b点所示溶液中c(A﹣)>c(HA)
D.pH=7时,c(Na+)﹣=c(A﹣)+c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B属于短周期中不同主族的元素,A、B原子的最外层电子中,成对电子和未成对电子占据的轨道数相等,若A元素的原子序数为a,则B元素的原子序数可能为( )
①a-4 ②a-5 ③a+3 ④a+4
A. ①④ B. ②③ C. ①③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍及其化合物在合金材料及催化剂等方面应用广泛。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,以下是从该矿渣中回收NiSO4的工艺流程:

已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3。
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是______________________。
(2)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为___________________,“浸渣”的成分除Fe2O3,FeO(OH)外还含有______________(填化学式)。
(3)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入SnC12将Fe3+还原为Fe2+,所需SnC12的物质的量不少于Fe3+物质的量的_____倍;除去过量的SnC12后,再用酸性K2Cr2O7标准溶液滴定溶液中的Fe2+,滴定时反应的离子方程式为____________。
(4)“浸出液”中c(Ca2+)=1.0×10-3mol,当除钙率达到99%时,除钙后的溶液中c(F-)=____mol·L-1[已知Ksp(CaF2)=4.0×10-11]。
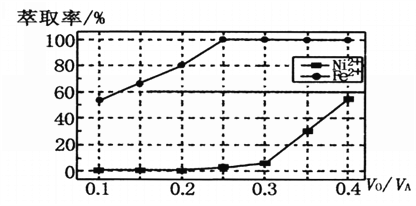
(5)本工艺中,萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(气体体积已折算为标准状况下的体积)。下列分析正确的是

A. OE段表示的平均速率最快
B. EF段,用盐酸表示该反应的平均反应速率为0.4mol/(L·min)
C. OE、EF、FG三段中,用二氧化碳表示该反应的平均反应速率之比为2:6:7
D. G点CO2不再增加的原因可能是盐酸的浓度过低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.
元素 | 结构或性质信息 |
X | 原子的L层上s电子数等于p电子数 |
Y | 原子核外的L层有3个未成对电子 |
Z | 地壳中含量最多的元素 |
Q | 单质常温常压下是气体,原子的M层上有1个未成对的p电子 |
R | 核电荷数是Y与Q的核电荷数之和 |
E | N能层上只有一个电子,K、L、M层均排满电子 |
请根据信息回答有关问题:
(1)写出元素Y的原子核外价电子排布图: . X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为 .
(2)X、Y、Z三种元素的第一电离能由高到低的排列为(写元素符号) .
(3)X、Z元素分别与氢元素形成的最简单化合物中,沸点较高的为(写化学式) , 原因是 .
(4)XZ与Y2属于等电子体,写出化合物XZ的结构式: .
(5)R的一种配合物的化学式为RCl36H2O.已知0.01mol RCl36H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此配合物最可能是 .
A.[R(H2O)6]Cl3
B.[R(H2O)5Cl]Cl2H2O
C.[R(H2O)4Cl2]Cl2H2O
D.[R(H2O)3Cl3]3H2O
(6)向含少量ESO4的水溶液中逐滴滴入氨水,生成蓝色沉淀,反应的离子方程式为: , 继续滴加氨水至过量,沉淀溶解, 得到天蓝色溶液,写反应的离子方程式为: .
(7)元素E的单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示. 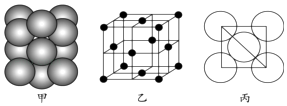
若已知该元素的原子半径为d cm,相对原子质量为M,NA代表阿伏加德罗常数,则该晶体的密度为gcm﹣3(用字母表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】节能减排、开发新能源目前受到国际社会的高度关注。
(1)近年我国努力开发新能源,调整能源结构。下列属于可再生能源的是_______(填字母)。
A.氢能 B.天然气 C.石油 D.生物质能
(2)工业生产中会产生SO2、H2S等有害气体,可采取多种方法进行处理。
I.生物法脱H2S的原理为:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4![]() 2Fe2(S04)3+2H2O
2Fe2(S04)3+2H2O
①硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是_______。
②由图1和图2判断使用硫杆菌的最佳条件为_____。若反应温度过高,反应速率下降,其原因是_____。

I.双碱法去除SO2的原理是先用NaOH溶液吸收SO2,再用CaO使NaOH再生。
NaOH溶液![]() Na2SO3溶液
Na2SO3溶液
写出过程①的离子方程式:______________。
(3)人们也利用多种方法回收利用烟气用的有害气体,变废为宝。如果利用NaOH溶液、石灰和O2处理硫酸工厂尾气中的SO2使之最终转化为石膏(CaSO4·2H2O),假设硫元素不损失,每天处理1000m3(标准状况)含0.2%(体积分数)SO2的尾气,理论上可以得到多少千克石膏 (计算结果保留小数点后一位)?_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
A.将Na2CO3固体加入新制的氯水中,有无色气泡(H+)
B.向淀粉KI溶液中滴加新制氯水,溶液变蓝(Cl2)
C.将AgNO3溶液滴加到新制氯水中,有白色沉淀产生(Cl﹣)
D.新制氯水使红色布条褪色(HCl)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标况下,下列物质中,与0.3moLH2O含相同氢原子数的物质是( )
A.0.6mol H2SO4
B.3.612×1023个HNO3分子
C.7.3g HCl
D.4.48L CH4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com