
| A、HF |
| B、HCN |
| C、HNO2 |
| D、CH3COOH |
科目:高中化学 来源: 题型:
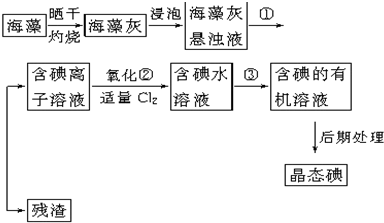 (1)指出提取碘的过程中有关的实验操作名称:①
(1)指出提取碘的过程中有关的实验操作名称:①查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、H+、OH-、Cl- |
| B、Cl-、NH4+、H+、OH- |
| C、H+、Cl-、NH4+、OH- |
| D、Cl-、NH4+、OH-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
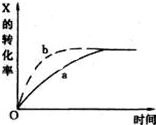 如图曲线a表示放热反应:X(g)+Y(g)?Z(g)+M(g)+N(s) 进行过程中x的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
如图曲线a表示放热反应:X(g)+Y(g)?Z(g)+M(g)+N(s) 进行过程中x的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )| A、升高温度 | B、加大X的投入 |
| C、加催化剂 | D、增大体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应容器内压强不随时间变化 |
| B、P和S的生成速率相等 |
| C、反应容器内P、Q、R、S四者共存 |
| D、反应容器内总物质的量不随时间而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2NO2=O2+2NO;△H=+1162kJ/mol |
| B、中和热:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=+57.3kJ/mol |
| C、燃烧热:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g);△H=-13670 kJ/mol |
| D、S(s)+O2(g)=SO2(g);△H=-2698kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com