
Mg(OH)2难溶于水,但它溶解的部分全部电离。室温下时,饱和Mg(OH)2溶液的pH=11,若不考虑KW的变化,则该温度下Mg(OH)2的溶解度是多少?(溶液密度为1.0 g·cm-3)
科目:高中化学 来源: 题型:
硅单质及其化合物应用范围很广.
(1)制备硅半导体材料必须先得到高纯硅,工业上可以按如下步骤制备纯硅.
Ⅰ.高温下用碳还原二氧化硅制得粗硅
Ⅱ.粗硅与干燥的氯气在450℃~500℃条件下反应制得SiCl4
Ⅲ.SiCl4液体经精馏提纯后与过量H2在1100℃~1200℃条件下反应制得纯硅
已知SiCl4沸点为57.6℃,能与H2O强烈反应.1 mol H2与SiCl4气体完全反应吸收的热量为120.2 kJ.
请回答下列问题:
①第Ⅲ步反应的热化学方程式是__________________ ____________________
____________________
_______________________________________________________________________。
②整个制备纯硅的过程中必须严格控制无水无氧.SiCl4在潮湿的空气中因水解而产生白色烟雾,其生成物是____________;H2还原SiCl4过程中若混入O2,可能引起的后果是____________.
③上述生产过程所需氯气和氢气均由氯碱厂提供,氯碱厂的基本设备是离子交换膜电解槽(如图所示),其中进入阳极室的溶液是__________________________________,b电极上的电极
反应式是______________________________________________________.

(2)二氧化硅被大量用于生产玻璃.工业上用SiO2、Na2CO3和CaCO3共283 kg在高温下完全反应时放出CO2 44 kg,生产出的玻璃可用化学式Na2SiO3·CaSiO3·xSiO2表示,则其中x=_____ ___。
___。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知铅蓄电池的工作原理为Pb+PbO2+2H2SO4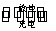
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移
0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题:
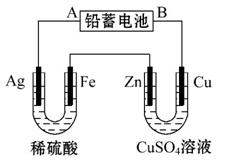
(1)A是铅蓄电池的 极,铅蓄电池正极反应式为 ,放电过程中电解液的密度 (填“减小”“增大”或“不变”)。
(2)Ag电极的电极反应式是 ,该电极的电极产物共 g。
(3)Cu电极的电极反应式是 ,CuSO4溶液的浓度 (填“减小”“增大”或“不变”)。
(4)如图表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示 。
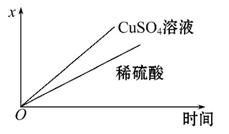
a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对沉淀溶解平衡的描述正确的是( )
A.反应开始时,溶液中各离子浓度相等
B.沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等
C.沉淀溶解达到平衡时,溶液中溶质的离子浓度相等,且保持不变
D.沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解下列溶液一段时间后再加入一定量的某种纯净物(方括号内的物质),能使溶液恢复到原来的成分和浓度的是( )
A.AgNO3[AgNO3] B.NaOH[H2O] C.KCl[KCl] D.CuSO4[Cu(OH)2]
查看答案和解析>>
科目:高中化学 来源: 题型:
按图甲装置进行实验,若图乙中横坐标x表示通过电极的电子的物质的量。下列叙述正确的是( )
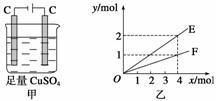
A.F表示反应生成Cu的物质的量
B.E表示反应实际消耗H2O的物质的量
C.E表示反应生成O2的物质的量
D.F表示反应生成H2SO4的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列浓度关系正确的是( )
A.氯水中:[Cl2]=2{[ClO-]+[Cl-]+[HClO]}
B. 氯水中:[Cl-]>[H+]>[OH-]>[ClO-]
C.等体积等浓度的氢氧化钠与醋酸混合:[Na+]=[CH3COO-]
D.Na2CO3溶液中:[Na+]>[CO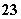 ]>[OH-]>[HCO
]>[OH-]>[HCO ]>[H+]
]>[H+]
查看答案和解析>>
科目:高中化学 来源: 题型:
已知N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·mol-1,下列结论正确的是( )
A.在密闭容器中加入1 mol N2和3 mol H2充分反应放热92.4 kJ
B.N2(g)+3H2(g)2NH3(l) ΔH=-Q kJ·mol-1,则Q>92.4
C.增大压强,平衡向右移动,平衡常数增大
D.若一定条件下反应达到平衡,N2的转化率为20%,则H2的转化率一定为60%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com