
【题目】实验室用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备碱式碳酸铜的主要实验流程如下。

(1)滤渣Ⅰ的成分为MnO2、单质S和 (写化学式);硫酸浸取时,Cu2S被MnO2氧化的化学方程式为 。
(2)浸取时,Fe2O3溶于硫酸的离子方程式为 ;研究发现若先除铁再浸取,浸取速率明显变慢,其可能原因是 。
(3)“赶氨”时,最适宜的操作方法是 。
(4)滤液Ⅱ经蒸发结晶得到的盐主要是 (写化学式)。
【答案】(1)SiO2;2MnO2 + Cu2S + 4H2SO4 = 2MnSO4 + 2CuSO4 +S+4H2O
(2)Fe2O3+6H+=2Fe3++3H2O;Fe3+可催化Cu2S被MnO2氧化(或答:Fe2O3在浸取时起媒介作用)
(3)将溶液加热(4)(NH4)2SO4
【解析】
试题分析:(1)辉铜矿中含有Cu2S、Fe2O3、SiO2,加入 H2SO4 和 MnO2 后,Cu2S 中+1 的 Cu 和-2 价的 S 均被氧化生成 Cu2+和 S,Fe2O3 溶解生成 Fe3+,SiO2 不溶于 H2SO4,故滤渣中还含有 SiO2。Cu2S 在 H2SO4 作用下,被 MnO2 氧化, 产物有 S、CuSO4、MnSO4 和 H2O,根据化合价升降总值相等得,其反应的化学方程式2MnO2 + Cu2S + 4H2SO4 = 2MnSO4 + 2CuSO4 +S+4H2O。 (2)Fe2O3 为难溶的氧化物,浸取时,Fe2O3溶于硫酸的离子方程式为Fe2O3+6H+=2Fe3++3H2O;由题意分析知,除铁后速率 变慢,说明 Fe3+对浸取速率是有影响的,可联想到 Fe3+可能作催化剂。(3)此处考查 NH3 具有挥发性的性质,以及[Cu(NH3)4]2+受热分解为 Cu2+ 和 NH3,故采用加热的方法可将 NH3 从溶液中赶出。(4)分析流程图,第一步中加入了 H2SO4,在整个过程中,没有除SO42- ,阳离子Fe3+、Mn 均以沉 淀形式除去,Cu2+进入主产物碱式碳酸铜中,所以滤液中应含有 NH4+ ,故蒸发得到的盐为(NH4)2SO4。


科目:高中化学 来源: 题型:
【题目】下列各组中化合物的性质比较,不正确的是( )
A. 酸性:HClO4>HBrO4>HIO4
B. 稳定性:PH3>H2S> HCl
C. 碱性:NaOH>Mg(OH)2>Al(OH)3
D. 非金属性F>O>S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是( )
A.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2bkJ/mol
B.C2H2(g)+![]() O2(g)═2CO2(g)+H2O(l)△H=2bkJ/mol
O2(g)═2CO2(g)+H2O(l)△H=2bkJ/mol
C.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4bkJ/mol
D.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=bkJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
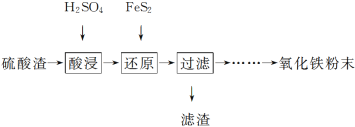
(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率。② 。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO![]() ,该反应的离子方程式为 。
,该反应的离子方程式为 。
(3)为测定“酸浸”步骤后溶液中Fe3+的量,以控制加入FeS2的量。实验步骤为准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应方程式如下:
2Fe3++Sn2++6Cl-===2Fe2++SnCl![]()
Sn2++4Cl-+2HgCl2===SnCl![]() +Hg2Cl2↓
+Hg2Cl2↓
6Fe2++Cr2O![]() +14H+===6Fe3++2Cr3++7H2O
+14H+===6Fe3++2Cr3++7H2O
①若SnCl2不足量,则测定的Fe3+量 (填“偏高”、“偏低”或“不变”,下同)
②若不加HgCl2,则测定的Fe3+量 。
(4)①可选用 (填试剂)检验滤液中含有的Fe3+。产生Fe3+的原因是 (用离子方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | Mn(OH)2 |
开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
实验可选用的试剂有:稀HNO3、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。
请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化: ;
b.沉淀: ;
c.过滤,洗涤;
d.烘干,研磨。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人胃酸(主要成分是盐酸)过多,会引起很多胃病。下图为某抗酸药包装标签上的部分文字,请回答下列问题。

(1)该药“嚼碎后吞服”的原因是_____________________。
(2)某同学为测定该药中氢氧化铝的质量分数进行如下几步操作:取一片药片(药片质量为0.5g),研碎后加20mL蒸馏水,然后用质量分数为5%,密度为1.02g/mL的盐酸进行反应(假设其他成分不与盐酸反应),测得实验中反应掉的盐酸体积为6.0mL。通过计算:
①判断该药片中氢氧化铝的含量是否与标签相符;
②确定该药片中氢氧化铝的质量分数为多少。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铝粉与Fe3O4粉末配制成铝热剂,分成三等份。
①一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为V1;
②一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为V2;
③一份直接放入足量的盐酸中,充分反应后放出气体在标准状况下的体积为V3。
下列说法正确的是
A.V1=V3>V2 B.V2>V1 =V3 C.V1= V2>V3 D.V1>V3>V2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含同一元素的常见物质A、B、C,有如下转化关系(条件未标注):
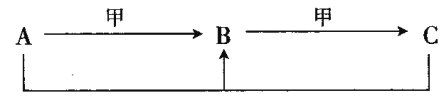
(1)当甲是KOH时,白色沉淀B为_____________。
(2)当甲为H2O时,气体B为______________。
(3)当A为Na时,单质甲为________________。
(4)当A为NH3时,气体单质B为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于常见有机物的说法不正确的是( )
A.乙烯和苯都能与溴水反应
B.乙酸和油脂都能与氢氧化钠溶液反应
C.糖类和蛋白质都是人体重要的营养物质
D.乙烯和甲烷可用酸性高锰酸钾溶液鉴别
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com