
 ��CΪHOOC-COOH��A�ĺ������ͼ�ͺ˴Ź�������ͼ��ͼ1��
��CΪHOOC-COOH��A�ĺ������ͼ�ͺ˴Ź�������ͼ��ͼ1��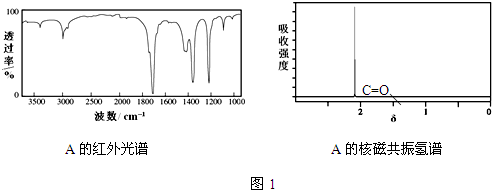

 ��
������ ��1��30.4g�л���X�����ʵ���Ϊ$\frac{30.4g}{152g/mol}$=0.2mol����ȫȼ�գ�����88g������̼��28.8gˮ����2mol������̼��1.6molˮ������1molX�к���10molCԭ�Ӻ�16molHԭ�ӣ�����Է�������Ϊ152��Ӧ�û���Oԭ�Ӹ���Ϊ$\frac{152-12��10-16��1}{16}$=1���ݴ˷��������ʽ��
��2��X�м���������Ȼ�̼��Һ����Һ��ɫ������������Һ������ˮԡ�����ȣ��۲쵽����������������KMnO4������Һ����ɫ���õ�������������A��B��C��������������ͺ˴Ź�������������������BΪ 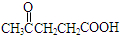 ��CΪHOOC-COOH����֪X�к���̼̼˫����ȩ����
��CΪHOOC-COOH����֪X�к���̼̼˫����ȩ����
��3����A�ĺ������ͼ�ͺ˴Ź�������ͼ��֪��A��ֻ��1��Hԭ���Һ���C=O����
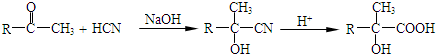
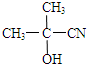
��4���ݹ�ҵ����AΪԭ�Ͻ��кϳ��л������ĺϳ�·��ͼ��֪��A��HCN�����ӳɷ�Ӧ���ɵ�MΪ ��
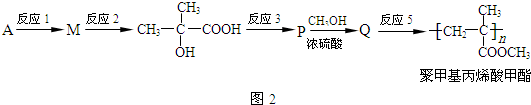
�� ˮ������2-��-2-�ǻ����ᣬ2-��-2-�ǻ����ᷢ����ȥ��Ӧ����2-����ϩ�ᣬ2-����ϩ����״�����������Ӧ���ɵ�QΪCH2=C��CH3��COOCH3��Q�����Ӿ۷�Ӧ���ɾۼ���ϩ�������
ˮ������2-��-2-�ǻ����ᣬ2-��-2-�ǻ����ᷢ����ȥ��Ӧ����2-����ϩ�ᣬ2-����ϩ����״�����������Ӧ���ɵ�QΪCH2=C��CH3��COOCH3��Q�����Ӿ۷�Ӧ���ɾۼ���ϩ�������
��� �⣺��1��30.4g�л���X�����ʵ���Ϊ$\frac{30.4g}{152g/mol}$=0.2mol����ȫȼ�գ�����88g������̼��28.8gˮ����2mol������̼��1.6molˮ������1molX�к���10molCԭ�Ӻ�16molHԭ�ӣ�����Է�������Ϊ152��Ӧ�û���Oԭ�Ӹ���Ϊ$\frac{152-12��10-16��1}{16}$=1�����������ʽΪC10H16O���ʴ�Ϊ��C10H16O��
��2��X�м���������Ȼ�̼��Һ����Һ��ɫ������������Һ������ˮԡ�����ȣ��۲쵽����������������KMnO4������Һ����ɫ���õ�������������A��B��C��������������ͺ˴Ź�������������������BΪ 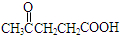 ��CΪHOOC-COOH����֪X�к���̼̼˫����ȩ����̼̼˫���ܹ������ӳɷ�Ӧ��ȩ�����ܹ�������ԭ��Ӧ���ܹ�����������Ӧ���ʴ�Ϊ��̼̼˫����ȩ����acd��
��CΪHOOC-COOH����֪X�к���̼̼˫����ȩ����̼̼˫���ܹ������ӳɷ�Ӧ��ȩ�����ܹ�������ԭ��Ӧ���ܹ�����������Ӧ���ʴ�Ϊ��̼̼˫����ȩ����acd��
��3����A�ĺ������ͼ�ͺ˴Ź�������ͼ��֪��A��ֻ��1��Hԭ���Һ���C=O����X�к���10��Cԭ�ӣ������Ը��������������BΪ 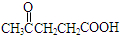 ��CΪHOOC-COOH��A������AΪCH3COCH3���ʴ�Ϊ��CH3COCH3��
��CΪHOOC-COOH��A������AΪCH3COCH3���ʴ�Ϊ��CH3COCH3��
��4���ݹ�ҵ����AΪԭ�Ͻ��кϳ��л������ĺϳ�·��ͼ��֪��A��HCN�����ӳɷ�Ӧ���ɵ�MΪ ��
�� ˮ������2-��-2-�ǻ����ᣬ2-��-2-�ǻ����ᷢ����ȥ��Ӧ����2-����ϩ��CH2=C��CH3��COOH��CH2=C��CH3��COOH��״�����������Ӧ���ɵ�QΪCH2=C��CH3��COOCH3��Q�����Ӿ۷�Ӧ���ɾۼ���ϩ��������ʴ�Ϊ����
ˮ������2-��-2-�ǻ����ᣬ2-��-2-�ǻ����ᷢ����ȥ��Ӧ����2-����ϩ��CH2=C��CH3��COOH��CH2=C��CH3��COOH��״�����������Ӧ���ɵ�QΪCH2=C��CH3��COOCH3��Q�����Ӿ۷�Ӧ���ɾۼ���ϩ��������ʴ�Ϊ���� ����CH2=C��CH3��COOH��
����CH2=C��CH3��COOH��
���� ���⿼���л�����ƶϣ���Ŀ�Ѷ��еȣ�����Ĺؼ����Ǹ��ݾۼ���ϩ�����Ϊ�����㣬������ʵĹ����ŵı仯�����ƶϣ�ע����չ����ŵ����ʣ�


 Ӣ�ŵ��ϵ�д�
Ӣ�ŵ��ϵ�д� ������������Ծ�ϵ�д�
������������Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩʹ��ˮ�����Ը��������Һ��ɫ�����ڼӳɷ�Ӧ | |
| B�� | ���³�ѹ�»�����ϩ ��һ��������ˮ����ɫ���� ��һ��������ˮ����ɫ���� | |
| C�� | �������ظ������Һ����Ƽݣ������ķ�Ӧ�����Ҵ���������Ӧ | |
| D�� | ����������ϩ���Ҵ���ȫȼ�գ�����O2�����ʵ�����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����ӵ����幹����ƽ�������Σ�
�����ӵ����幹����ƽ�������Σ� ����CCl4��Ϊ�ȵ�����ķ��Ӻ����ӷֱ���SiCl4��SO42-������һ����д��ѧʽ����
����CCl4��Ϊ�ȵ�����ķ��Ӻ����ӷֱ���SiCl4��SO42-������һ����д��ѧʽ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ԭ��������Ar��K | B�� | ���ԣ�NaOH��Mg��OH��2 | ||
| C�� | ���ԣ�HNO3��H3PO4 | D�� | Ԫ�طǽ����ԣ�Cl��S |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƾ���ȼ����AH=-Q3 kJ•mol-1 | |
| B�� | �ɢۿ�֪1molC2H5OH��g������������2molC02��g����3 molH20��g���������� | |
| C�� | H20��g����H20�� 1���ͷų������������Ըù���Ϊ���ȷ�Ӧ | |
| D�� | 23gҺ��ƾ���ȫȼ������C02��g����H20�� 1�����ͷ�����Ϊ��0.5Q3-0.5Q2+1.5Q1��kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��A��=0.15mol/��L•min�� | B�� | v��B��=0.3 mol/��L•min�� | ||
| C�� | v��C��=0.2 mol/��L•min�� | D�� | v��D��=0.1 mol/��L•min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
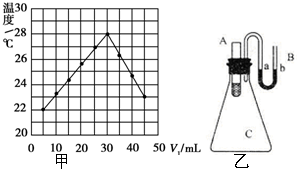 ʵ���⣺��V1 mL 1.0mol•L-1HCl��Һ��V2 mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ������ͼ��ʾ��ʵ����ʼ����V1+V2=50mL�����밴Ҫ����գ�
ʵ���⣺��V1 mL 1.0mol•L-1HCl��Һ��V2 mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ������ͼ��ʾ��ʵ����ʼ����V1+V2=50mL�����밴Ҫ����գ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ۢܢݢ� | B�� | �ڢۢܢ� | C�� | �٢ۢܢ� | D�� | �ۢܢޢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ۼ����м���֮˵��������ָ��1mol���ۼ�����Ҫ���յ��������γ�1mol���ۼ����ų���������
���ۼ����м���֮˵��������ָ��1mol���ۼ�����Ҫ���յ��������γ�1mol���ۼ����ų���������| ��ѧ�� | H-H | H-F | H-Cl | H-Br |
| ����/kJ/mol | 436 | 565 | 431 | 368 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com