
| A. | 1-丙醇制丙烯;丙烯与溴水反应制1,2-二溴丙烷 | |
| B. | 溴乙烷水解制丙醇;丙烯与水反应制丙醇 | |
| C. | 甲苯硝化制对硝基甲苯;甲苯氧化制苯甲酸 | |
| D. | 乙酸和乙醇制乙酸乙酯;苯甲酸乙酯水解制苯甲酸和乙醇 |
分析 A.1-丙醇制丙烯的反应为消去反应;丙烯与溴水反应制1,2-二溴丙烷为加成反应;
B.溴乙烷水解制丙醇为取代反应;丙烯与水反应制丙醇为加成反应;
C.甲苯硝化制对硝基甲苯为取代反应;甲苯氧化制苯甲酸为氧化反应;
D.乙酸和乙醇制乙酸乙酯;苯甲酸乙酯水解制苯甲酸和乙醇,两个反应都是取代反应.
解答 解:A.1-丙醇制丙烯;丙烯与溴水反应制1,2-二溴丙烷,前者为消去反应,后者为加成反应,两个反应类型不同,故A错误;
B.溴乙烷水解制丙醇;丙烯与水反应制丙醇,前者为取代反应,后者为加成反应,两个反应类型不同,故B错误;
C.甲苯硝化制对硝基甲苯;甲苯氧化制苯甲酸,前者为取代反应,后者为氧化反应,反应类型不同,故C错误;
D.乙酸和乙醇制乙酸乙酯为酯化反应,也属于取代反应;苯甲酸乙酯水解制苯甲酸和乙醇为酯的水解反应,属于取代反应,两个反应的类型相同,故D正确;
故选D.
点评 本题考查了有机反应类型的判断,题目难度不大,明确发生反应的实质为解答关键,注意掌握常见有机反应概念、类型及判断方法,试题侧重基础知识的考查,培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
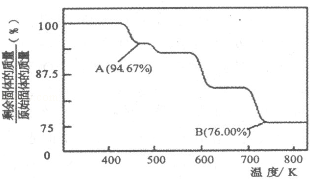 铬是用途广泛的金属,但在生产过程中易产生有害的含铬工业废水.
铬是用途广泛的金属,但在生产过程中易产生有害的含铬工业废水.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ①②③⑤ | C. | ①②③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 45mL | B. | 180mL | C. | 90mL | D. | 135mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L0.5mol/LNaHCO3溶液中HCO3-的数目小于0.5 NA | |
| B. | 1mol-OH和1molOH-所含电子数为NA | |
| C. | 25℃时,0.1mol/LKOH溶液中含有OH-的数目为0.1NA | |
| D. | 78g苯中含有碳酸双键的数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1:4.3×10-7 K2:5.6×10-11 | 3.2×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(SO42-)≈c(CrO42-) | B. | c(SO42-)>c(CrO42-) | C. | c(SO42-)<c(CrO42-) | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 利用下列各组中的物质制备并收集少量相应的气体,能采用如图装置的是(2)(3)(9)
利用下列各组中的物质制备并收集少量相应的气体,能采用如图装置的是(2)(3)(9)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于0.6mol | B. | 等于0.15mol | ||
| C. | 介于0.15mol与0.3mol之间 | D. | 等于0.3mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com