
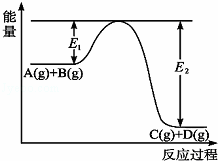
反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
(1)该反应是 (填“吸热”或“放热”)反应.
(2)当反应达到平衡时,升高温度,A的转化率减小(填“增大”“减小”或“不变”),原因是 .
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1 ,E2 (填“增大”“减小”或“不变”).
考点: 反应热和焓变;化学平衡的影响因素.
专题: 化学平衡专题.
分析: (1)分析图象中物质能量变化可知AB反应物能量高于生成物CD,反应是放热反应;
(2)反应前后气体体积不变,增大压强平衡不动,A的转化率不变;
(3)催化剂能同等程度地改变正逆反应速率,减小反应的活化能.
解答: 解:(1)分析图象中物质能量变化可知AB反应物能量高于生成物CD,反应是放热反应,A(g)+B(g)⇌C(g)+D(g)过程中的能量变化为放热,
故答案为:放热;
(2)A(g)+B(g)⇌C(g)+D(g)反应为放热反应,升高温度平衡逆向移动,A的转化率减小,
故答案为:减小;升温,平衡逆向移动;
(3)其它条件不变在反应体系中加入催化剂,能同等程度地改变正逆反应速率,降低了反应的活化能,反应物和生成物的活化能都会降低,
故答案为:E1减小,E2减小.
点评: 本题考查了化学反应能量变化的分析判断,影响化学平衡的因素分析,注意催化剂改变反应速率不改变化学平衡,题目较简单.答题:


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
已知下列热化学方程式:
Zn(s)+O2(g)═ZnO(s)△H=﹣Q1 kJ/mol
Hg(l)+O2(g)═HgO(s)△H=﹣Q2kJ/mol
Zn(s)+HgO(s)═Hg(l)+ZnO(s)△H=﹣Q3kJ/mol
Q3值为()
A. Q2﹣Q1 B. Q1+Q2 C. Q1﹣Q2 D. ﹣Q1﹣Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表中,同主族元素从上到下,原子半径逐渐 (填“增大”或“减小”),元素的金属性逐渐 (填“增强”或“减弱”),非金属性逐渐 (填“增强”或“减弱”);同周期从左到右,原子半径逐渐 (填“增大”或“减小”),元素的金属性逐渐 (填“增强”或“减弱”),非金属性逐渐 (填“增强”或“减弱”).
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应可视为旧键的断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(KJ•mol﹣1)P﹣P:198 P﹣O:360 O=O:498 则反应P4(白磷)+3O2→P4O6 的反应热△H为()

A. +1638KJ•mol﹣1 B. ﹣1638KJ•mol﹣1
C. +126KJ•mol﹣1 D. ﹣126KJ•mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下的密闭容器中,当下列物理量不再变化时,表明A(s)+2B(g)⇌C(g)+D(g)已达平衡的是()
A. 混合气体的压强 B. 混合气体的密度
C. 混合气体的分子数目 D. 混合气体的总物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在生产和日常生活中有着重要的应用.下列说法不正确的是()
A. 铝盐(明矾溶液)和铁盐(硫酸铁溶液)都有净水作用,两者的作用原理是相同的
B. 放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关
C. 0.1mol/L的CH3COONa溶液的pH约为9,说明CH3COOH是弱酸
D. 室温下向10mLpH=3的醋酸溶液中加入水稀释后,溶液中导电粒子的数目减少
查看答案和解析>>
科目:高中化学 来源: 题型:
如图,在盛有稀 H2SO4 的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是()
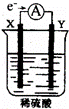
A. 外电路的电流方向为:X→外电路→Y
B. 若两电极分别为Fe和碳棒,则X为碳棒,Y为Fe
C. X极上发生的是还原反应,Y极上发生的是氧化反应
D. 若两电极都是金属,则它们的活动性顺序为X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
有一环保汽车,是以氢气作燃料的,请按题目要求作答:
(1)氢气在发动机内燃烧过程中,生成物只有水蒸气,不会使空气中的 含量偏高,因而能减缓温室效应现的发生.
(2)如果每mol氢气燃烧后生成水蒸气并放出241.8kJ的热量,写出氢气燃烧的热化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com