
A.![]() B.
B.![]()
C.![]() D.
D.![]()
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:黄冈重点作业 高一化学(下) 题型:013
已知某元素的阴离子 的核内中子数为A-x+n,其中A为R原子的质量数,则mg
的核内中子数为A-x+n,其中A为R原子的质量数,则mg  中所含电子总数(设
中所含电子总数(设 为阿伏加德罗常数)为
为阿伏加德罗常数)为
[ ]

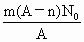


查看答案和解析>>
科目:高中化学 来源:设计必修二化学人教版 人教版 题型:022
已知某元素R原子的质量数为A,其阴离子Rn-含有x个电子,则m g Rn-中含中子的物质的量是________mol.
查看答案和解析>>
科目:高中化学 来源:山东省莘县第二中学2009-2010学年高一下学期期末模拟考试化学试题 题型:022
(1)写出表示含有8个质子,10个中子的原子的化学符号:________;
(2)已知阴离子aX2-和阳离子bYn+具有相同的核外电子排布,则a、b、n之间的关系为a=________;
(3)比较下列大小(填“>”“<”)
A.原子半径:Cl________Na
B.酸性:H2CO3________H2SiO3;
(4)某元素R气态氢化合物的化学式RH3,其最高价氧化物中含氧20/27,已知该元素的原子核中中子数和质子数相等,则该元素的名称是________;
(5)反应A+3B=2C+2D在四种不同的情况下的反应速率分别如下,该反应进行的快慢顺序为________.
①V(A)=0.15 mol/(L·S)
②V(B)=0.6 mol/(L·S)
③V(C)=0.5 mol/(L·S)
④V(D)=0.45 mol/(L·S)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com