
17.(共6分)金属Na、Mg、Al有广泛的应用。
(1)周期表中Na、Mg、Al所在周期是 。
(2)为比较Na、Mg、Al的金属性,进行了如下实验:
实验1:各取1.0 g金属钠和镁,分别加入到5 mL水中,钠与水反应剧烈,镁与水反应缓慢。
实验2:各取1.0 g的镁条和铝条,分别加入到5 mL 1.0 mol/L盐酸中,镁与盐酸反应剧烈,铝与盐酸反应较剧烈。
已知:元素金属性强弱可以从其单质与水(或酸)反应置换出氢的难易程度来判断。
由实验1和实验2得出的结论是 ,用原子结构理论解释:同周期元素从左到右, 。
(3)Na、Mg、Al都可以用于制备储氢的金属氢化物。
① NaH是离子化合物,能与水发生氧化还原反应生成H2,该反应的还原剂是 。
② NaAlH4是一种良好的储氢材料。NaAlH4与水反应的化学方程式是 。
(1)第三周期
(2)金属性Na>Mg>Al;原子半径逐渐减小,失电子能力逐渐减弱
(3)①NaH
②NaAlH4+2H2O=NaAlO2+4H2↑
【解析】
试题分析:(1)钠、镁、铝分别为11、12、13号元素,原子核外有3个电子层,处于周期表的饿第三周期;(2)实验1:取1.0 g金属钠和镁,分别加入到5 mL水中,钠与水反应剧烈,镁与水反应缓慢,说明钠比镁活泼;实验2:取1.0 g的镁条和铝条,分别加入到5 mL 1.0 mol/L盐酸中,镁与盐酸反应剧烈,铝与盐酸反应较剧烈,说明镁比铝活泼,综上可得结论:金属的活泼性Na>Mg>Al;同周期从左到右,原子半径逐渐减小,是电子能力逐渐减弱;(3)①NaH是离子化合物,Na为+1价,H为-1价,与水发生了氧化还原反应后-1价的H变为0价,化合价升高,被氧化,自身作还原剂,故反应的还原剂为NaH;② NaAlH4是一种良好的储氢材料,NaAlH4中Na为+1价,Al为+3价,H为-1价,发生氧化还原反应后产生H2的同时,生成NaAlO2,NaAlH4与水反应的化学方程式是为NaAlH4+2H2O=NaAlO2+4H2↑。
考点:元素周期律


科目:高中化学 来源:2014-2015天津市和平区高一上学期期末考试化学试卷(解析版) 题型:填空题
(1)某建筑材料,主要成分铝硅酸盐,化学式MgAl2H4Si4O14;化学式改写成氧化物形式为_____________。则材料该与足量的氢氧化钠反应后过滤,滤渣主要是______.写出该过程中发生的离子方程式_______________________________、_______________________________________。
(2)检验CO2中是否混有SO2可将气体通过盛有______的洗气瓶.
(3)鉴别Na2CO3和NaHCO3溶液可选用______(填序号).
①NaOH ②Ca(OH)2 ③BaCl2④K2SO4 ⑤Ca(NO3)2
(4)某溶液中有NH4+,Mg2+,Fe2+,Al3+四种离子,若向其中加入过量的氢氧化钠溶液,加热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是______.
A.NH4+ B.Mg2+ C.Fe2+ D.Al3+
(5)6.4gCu与过量硝酸(60mL 8mol/L)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中所含H+为n mol,NO、NO2混合气体的物质的量为________________
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省绵阳市高一上学期期末化学试卷(解析版) 题型:选择题
新制氯水与久置氯水相比较,下列说法错误的是
A.颜色不同 B.都能使滴有酚酞的NaOH溶液褪色
C.都能使有色布条褪色 D.加AgNO3溶液都能生成白色沉淀
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省高三上学期第五次月考理综化学试卷(解析版) 题型:选择题
13.R、X、Y、M、Z五种短周期主族元素的原子半径依次减小,X、Y、Z的电子层数之和为5,X元素原子的最外层电子数是它的电子层数的2倍,Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,M是地壳中含量最多的元素,R与Z的最外层电子数相同下列叙述正确的是
A.Z与M形成的化合物中不可能含有非极性键
B.对应氢化物的热稳定性:X > Y >M
C.单质的还原性:R> M>Y>X
D.X、Y、M、Z四种元素组成的离子化合物受热易分解
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市西城区高三上学期期末考试化学试卷(解析版) 题型:推断题
22.(16分)华法林是一种治疗心脑血管疾病的药物,其合成路径如下(部分反应条件略去)。

已知:

(1)A属于芳香烃,名称是 。
(2)B→C的化学方程式是______。
(3)D的含氧官能团名称是______。
(4)E的结构简式是______。
(5)F→K的化学方程式是______。
(6)由E与N合成华法林的反应类型是______。
(7)下列说法正确的是______。
a.M与N互为同分异构体
b.将L与足量的NaOH溶液反应,1 mol L消耗4 mol NaOH
c.E最多可与5 mol氢气加成
d.B可以发生消去反应
(8)L→M的转化中,会产生少量链状高分子聚合物,该反应的化学方程式是______。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市西城区高三上学期期末考试化学试卷(解析版) 题型:选择题
12.分别依据下列实验事实,得出的结论正确的是
实验事实 | 结论 | |
A | 苯酚和水的浊液中,加碳酸钠溶液,溶液变澄清 | 苯酚的酸性比碳酸强 |
B | 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快褪为无色 | 随溶液pH减小,“84”消毒液的氧化能力增强 |
C | 铜放入稀硫酸中,无明显现象,再加入硝酸钠固体,溶液变蓝,有明显的气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
D | 向2 mL 0.1 mol/L的硝酸银溶液中加入1 mL0.1 mol/L NaCl溶液,出现白色沉淀,再加入几滴0.1 mol/L Na2S溶液,有黑色沉淀生成 | 氯化银的溶解度大于硫化银 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市西城区高三上学期期末考试化学试卷(解析版) 题型:选择题
5.下列有关钢铁腐蚀与防护的说法不正确的是
A.生铁比纯铁容易生锈
B.钢铁的腐蚀生成疏松氧化膜,不能保护内层金属
C.钢铁发生吸氧腐蚀时,正极反应式为:O2+2H2O+4e-== 4OH-
D.为保护地下钢管不受腐蚀,可使其与直流电源正极相连
查看答案和解析>>
科目:高中化学 来源:2015-2015湖南省高二12月学科联赛化学试卷(解析版) 题型:选择题
9.现有分别放置下图装置(都盛有稀H2SO4溶液)中的四个相同的纯锌片,腐蚀最慢的是
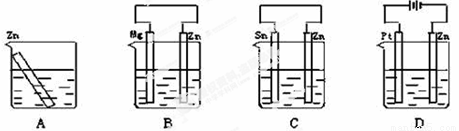
查看答案和解析>>
科目:高中化学 来源:2014-2015云南省景洪市高一上学期期中化学试卷(解析版) 题型:选择题
20.下列变化需要加入还原剂才能实现的转化是
A.浓H2SO4→SO2 B.Fe2+→Fe3+
C.H2S→SO2 D.HCO3-→CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com