
【题目】实验室配制氯化亚铁溶液时,为了防止其氧化,常加入的物质是
A. Fe B. Zn C. Al D. HCl
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行了有关Cu、硝酸、硫酸化学性质的实验,实验过程如下图所示。下列有关说法正确的是
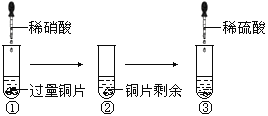
A. 实验①中溶液呈蓝色,试管口有红棕色气体产生,说明稀硝酸被Cu还原为NO2
B. 实验③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强
C. 实验③发生反应的化学方程式为:3Cu+Cu(NO3)2+4H2SO4=4CuSO4+2NO↑+4H2O
D. 由上述实验可得出结论:Cu在常温下既可以和稀硝酸反应,也可以和稀硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表是元素周期表的一部分,请回答有关问题:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为 .
(2)表中能形成两性氢氧化物的元素是(用元素符号表示),写出该元素的单质与⑨最高价氧化物对应水化物反应的化学方程式 .
(3)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入如表.
实验步骤 | 实验现象与结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25℃、l0lkPa条件下
4Al(s)+3O2(g)=2Al2O3(s) ΔH=-2834.9kJ/mol
4Al(s)+2O3(g)=2Al2O3(s) ΔH=-3119.91kJ/mol: 由此得出的结论正确的是
A. 等质量的O2比O3能量低,由O2变O3为吸热反应
B. 等质量的O2比O3能量低,由O2变O3为放热反应
C. O3比O2稳定,由O2变O3为吸热反应
D. O2比O3稳定,由O2变O3为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属说法正确的是
A. 自然界中的金属元素都以化合态存在
B. 金属钠着火,可以用水灭火
C. 铁在潮湿的空气中很稳定,但红热的铁丝可与水蒸气反应
D. Al与NaOH溶液的反应中,每转移3mole-,就生成1.5molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】复分解反应是中学化学中常见的一种反应类型。复分解反应中,元素的化合价都没发生变化,都不属氧化还原反应。
(1)复分解反应存在这样一个规律:一种较强酸与另一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐。已知相同物质的量浓度的溶液,pH大小关系是pH(Na2CO3)>pH(NaClO)>pH(NaHCO3)>pH(NaHS O3)。
①写出向NaClO溶液中通入少量CO2的化学方程式______________________。
②将混有CO2气体的SO2气体,通入NaHSO3饱和溶液,___________(填“能”或“不能”)除去CO2气体。
(2)复分解反应从形式上看,是一种相互交换成分的反应,在有机反应中,也存在类似形式的反应——“烯烃的复分解”反应。

如果用重氢(D)标记过的烯烃CD3CD![]() CDCD3和烃CH3CH
CDCD3和烃CH3CH![]() CHCH3进行反应,其化学方程式是______________________。
CHCH3进行反应,其化学方程式是______________________。
(3)复分解反应的发生还遵循向生成沉淀、气体、难电离物质的方向进行。
①甲同学认为CuSO4+H2S![]() H2SO4+CuS↓不能发生,因为该反应违背了“较强酸制较弱酸”的原则。请你判断甲同学的观点是否正确,并做出解释:________________。
H2SO4+CuS↓不能发生,因为该反应违背了“较强酸制较弱酸”的原则。请你判断甲同学的观点是否正确,并做出解释:________________。
②乙同学认为,BaSO3可溶于酸,SO2通入Ba(NO3)2溶液中不发生化学反应,但经过实验探究发现,有白色沉淀生成,请你写出相关反应的离子方程式_____________。
(4)电解是一种在通电作用下的氧化还原反应。用电解法可将某工业废水中的CN-转变为N2,装置如上图所示。电解过程中,阴极区电解质溶液的pH将_____________(填“增大”“减小”或“不变”)。阳极的电极反应式为______________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲除去甲烷气体中混有的乙烯得到纯净的甲烷,最好依次通过盛有( )试剂的装置.
A.澄清石灰水、浓H2SO4
B.酸性KMnO4溶液、浓H2SO4
C.溴水、浓H2SO4
D.CCl4、碱石灰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com