
| A. | $\frac{22.4b}{5a}$ | B. | $\frac{5a}{11.2b}$ | C. | $\frac{22.4a}{5b}$ | D. | $\frac{11.2b}{5a}$ |
分析 发生反应:4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O,反应中N元素化合价由-3价升高为+2价,根据n=$\frac{V}{Vm}$计算氨气物质的量,结合N元素化合价变化表示出电子数目,进而计算阿伏伽德罗常数.
解答 解:发生反应:4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O,反应中N元素化合价由-3价升高为+2价,有标准状况下a L氨气完全反应,则转移电子数目为:$\frac{aL}{22.4L/mol}$×[2-(-3)]×NA=b,解得NA=$\frac{22.4b}{5a}$mol-1,故选A.
点评 本题考查阿伏伽德罗常数计算、氧化还原反应计算,关键是理解氧化还原反应中转移电子的计算,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 两种气体的分子个数之比为17:16 | |
| B. | 同温同压下,两种气体的体积之比为17:16 | |
| C. | 两种气体的氢原子个数之比为17:12 | |
| D. | 同温同压下,两种气体的密度之比为17:16 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 3,4-二甲基-4乙基-庚烷
3,4-二甲基-4乙基-庚烷 3-甲基-丁炔
3-甲基-丁炔 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向碳酸氢铵溶液中加入足量的氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| B. | 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| D. | Ca(ClO)2溶液中通入过量的二氧化硫气体:ClO-+SO2+H2O═HClO+HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgO、Al2O3熔点高,都可用于制作耐火材料 | |
| B. | 氨气显碱性,可用碱石灰或无水CaCl2干燥 | |
| C. | 氢氟酸具有强酸性,可用于雕刻玻璃 | |
| D. | 铜的活动性比铁弱,可在海轮外壳上装铜块以减缓海轮腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
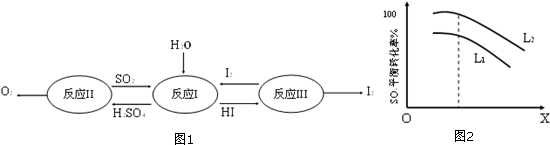
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
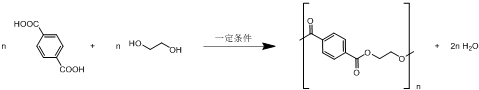 .
.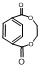 .
.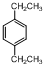 .
.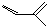 ,两分子该单体发生“Diels-Alder反应”,写出两种不同结构的产物
,两分子该单体发生“Diels-Alder反应”,写出两种不同结构的产物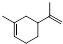 、
、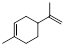 .
.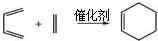
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
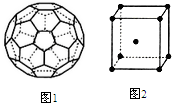 X、Y、Z、W、Q五种元素的原子序数依次增大,X、Y、Z、W属于短周期元素.已知X位于周期表的s区,其原子中电子层数和未成对电子数相同;Y原子核外有三个能级,且每个能级上容纳的电子数相同;W原子最外层电子数是次外层电子数的3倍;Q元素的原子核外有26个运动状态完全不相同的电子.回答下列问题:
X、Y、Z、W、Q五种元素的原子序数依次增大,X、Y、Z、W属于短周期元素.已知X位于周期表的s区,其原子中电子层数和未成对电子数相同;Y原子核外有三个能级,且每个能级上容纳的电子数相同;W原子最外层电子数是次外层电子数的3倍;Q元素的原子核外有26个运动状态完全不相同的电子.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com