
【题目】在溶液导电性实验装置里,分别注入20mL 6mol·L-1醋酸和20mL 6mol·L-1氨水,灯光明暗
程度相似,如果把这两种溶液混和后再试验则( )
A.灯光明暗程度不变 B.灯光变暗
C.灯光明暗程度变化不明显 D.灯光变亮
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在2L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2min末Z的平均反应速率分别为 ( )

A. X+3Y=2Z 0.1mol·min—1
B.2X+Y![]() 2Z 0.1mol·min—1
2Z 0.1mol·min—1
C.X+2Y=Z 0.05mol·min—1
D.3X+Y![]() 2Z 0.05mol·min—1
2Z 0.05mol·min—1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2SO2(g)+O2(g)=2SO3(g) △H,有关数据如下:

下列说法不正确的是( )
A.根据平衡常数随温度的变化关系,判断出△H<0
B.保持其他条件不变,SO2的平衡转化率a(727℃)<a(927℃)
C.增大压强、降低温度能提高SO2的转化率
D.SO3的稳定性随温度的升高而降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ca(ClO)2与浓盐酸反应会生成Cl2,该反应的化学方程式为:
Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
回答下列问题:
(1)浓盐酸在反应中显示出来的性质是________(填字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.3 mol Cl2,则转移的电子的物质的量为____________mol。
(3)此反应的离子方程式为_____________________。
(4)用双线桥法标出该反应的电子转移的方向和数目:_________________________。
(5)配平化学方程式:______KMnO4+_______HC1(浓)=_______KCl+_______MnCl2+_______Cl2↑+______H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”—全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法正确的是 ( )
A.分子中三个碳原子可能处于同一直线上
B.全氟丙烷的电子式为: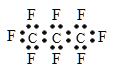
C.相同压强下,沸点:C3F8<C3H8
D.全氟丙烷分子中既有极性键又有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下列反应回答相应问题。
(1)3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O未被还原的硝酸与参加反应的总硝酸的质量比为 。
(2)S+2KNO3+3C![]() K2S+N2↑+3CO2↑ 还原剂是 还原产物是
K2S+N2↑+3CO2↑ 还原剂是 还原产物是
(3)3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O 反应中若消耗3molCl2共转移 mol电子
5NaCl+NaClO3+3H2O 反应中若消耗3molCl2共转移 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 需要加热才能发生的反应一定是吸热反应
B. 放热反应在常温下一定很容易发生
C. 判断反应是放热还是吸热必须看反应物和生成物具有的总能量的相对大小
D. 已知石墨(s)比金刚石(s)稳定,则石墨(s)转化为金刚石(s)要放出能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B.用小苏打治疗胃酸过多:HCO3-+H+= CO2↑+H2O
C.实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-![]() Cl2↑+Mn2++H2O
Cl2↑+Mn2++H2O
D.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu = Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了如下实验流程:在一个小烧杯里,加入20 g Ba(OH)2·8H2O晶体和10 g NH4Cl晶体,然后将小烧杯放在事先已滴有3~4滴水的玻璃片上,并立即用玻璃棒迅速搅拌。实验流程示意图如下,回答下列问题:
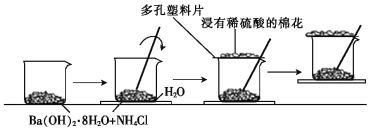
(1)实验中玻璃棒的作用是 。
(2)浸有稀硫酸的棉花的作用是 。
(3)通过 现象,说明该反应为 (填“吸热”或“放热”)反应,这是因为反应物的总能量 (填“>”“<”或“=”)生成物的总能量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com