
【题目】工业废气中的NO2、CO2对环境具有极大影响,利用化学反应原理对其处理,对构建“绿水青山”生态文明有重要意义。请回答下列问题:
(1)下列说法正确的是_________
A.CO2和NO2与水反应所得溶液均为弱酸
B.NO2在一定条件下能与NH3反应生成环境友好的物质
C.通过测定溶液的pH,一定能判断H2CO3和HNO2的酸性强弱
D.Na2CO3溶液中加入硫酸可生成CO2
(2)H2在催化剂存在下能与NO2反应生成水蒸气和氮气而消去工业尾气中NO2的污染,
已知:①N(g)+2O2(g)=2NO2(g)ΔH=+133kJ/mol;②H2O(g)=H2O(1)ΔH=-44kJ/mol;③H2的燃烧热为285.8kJ/mol,该反应的热化学方程式为___________.
(3)CO2可在一定条件下转化为CH3OH。己知向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂和T1温度下,发生反应:CO2(g)+3H2(g) ![]() CH3OH(1)+H2O(1)ΔH<O,10min时达到平衡状态,10min后改变温度为T2,生成物全部为气体,20min时达到平衡状态,反应过程中部分数据见表:
CH3OH(1)+H2O(1)ΔH<O,10min时达到平衡状态,10min后改变温度为T2,生成物全部为气体,20min时达到平衡状态,反应过程中部分数据见表:
反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
0min | 2 | 6 | 0 | 0 |
10min | 4.5 | |||
20min | 1 |
①前10min内的平均反应速率v(CO2)=_______,20min时H2的转化率为_______。
②在其他条件不变的情况下,若30min时只改变温度为T3,达平衡时H2的物质的量为3.2mol,则T2______T3(填“>”“<”或“=”),在温度T2时,反应的化学平衡常数为______。
③在T1温度下,将容器容积缩小一倍,反应达平衡时CH3OH物质的量为____mol.和改变下列条件,能使H2的反应速率和转化率都一定增大的是____(填标号)。
A.在容积不变下升高温度
B.其它条件下不变,增加压强
C.在容积和温度不变下充入N2
D.在容积和温度不变下及时分离出CH3OH
【答案】 BD 4H2(g)+2NO2(g)=N2(g)+4H2O(g) ΔH=-1100.2kJ/mol 0.025mol/(Lmin) 50% < 4/27 0.75 B
【解析】(1) A.CO2与水反应生成H2CO3,NO2与水反应生成HNO3和NO,HNO3为强酸,选项A错误;B.NO2具有氧化性,NH3具有还原性,两者在一定条件下能反应生成无污染的N2、H2O,选项B正确;C.由于物质的量浓度没有限定,无法根据两者的pH判断其酸性强弱,选项C错误;D.硫酸为强酸,能与弱酸盐Na2CO3反应生成CO2,选项D正确。答案选BD;(2)根据热化学方程式:①N2(g)+2O2(g)=2NO2(g)ΔH1=+133kJ/mol;②H2O(g)=H2O(1)ΔH2=-44kJ/mol;③H2的燃烧热为285.8kJ/mol:2H2(g)+O2(g)= 2H2O(1) ΔH3=-571.6kJ/mol;根据盖斯定律,由③×2-②×4-①可得反应:4H2(g)+2NO2(g)=N2(g)+4H2O(g) ΔH=ΔH3×2-ΔH2×4-ΔH1=-571.6kJ/mol×2-(-44kJ/mol)×4-(+133kJ/mol)=-1100.2kJ/mol;(3)①v(H2)= 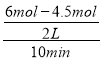 =0.075mol/(Lmin),速率之比等于化学计量数之比,v(CO2)=
=0.075mol/(Lmin),速率之比等于化学计量数之比,v(CO2)= ![]() v(H2)=
v(H2)= ![]() ×0.075mol/(Lmin)= 0.025mol/(Lmin);20min时消耗1molCO2,则消耗3molH2,H2的转化率=
×0.075mol/(Lmin)= 0.025mol/(Lmin);20min时消耗1molCO2,则消耗3molH2,H2的转化率=![]() ×100%=50%;②T2温度下平衡时氢气物质的量为3mol,在其他条件不变的情况下,若30min时只改变温度T3,达平衡时H2的物质的量为3.2mol,平衡逆向移动,氢气浓度增大,由于正反应为放热反应,可以升高温度,即T2<T3;20min时,转化的CO2为2mol-1mol=1mol,则生成的甲醇为1mol,
×100%=50%;②T2温度下平衡时氢气物质的量为3mol,在其他条件不变的情况下,若30min时只改变温度T3,达平衡时H2的物质的量为3.2mol,平衡逆向移动,氢气浓度增大,由于正反应为放热反应,可以升高温度,即T2<T3;20min时,转化的CO2为2mol-1mol=1mol,则生成的甲醇为1mol,
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
起始浓度(mol/L) 1 3 0 0
改变浓度(mol/L) 0.5 1.5 0.5 0.5
平衡浓度(mol/L) 0.5 1.5 0.5 0.5
故平衡常数K=![]() =
=![]() =
=![]() ;③T1温度下,生成物为液态,K=
;③T1温度下,生成物为液态,K=![]() 由于温度不变,K不变,容器容积缩小一倍,CO2浓度变为2mol/L、氢气浓度变为6mol/L,设此时达平衡时二氧化碳浓度为xmol/L,则:
由于温度不变,K不变,容器容积缩小一倍,CO2浓度变为2mol/L、氢气浓度变为6mol/L,设此时达平衡时二氧化碳浓度为xmol/L,则:
CO2(g)+3H2(g) ![]() CH3OH(1)+H2O(l)
CH3OH(1)+H2O(l)
起始浓度(mol/L) 2 6
改变浓度(mol/L) 2-x 6-3x
平衡浓度(mol/L) x 3x
则![]() =
=![]() ,解得x=0.75,生成甲醇物质的量为0.75mol;④A、升高温度,氢气的反应速率增大,但该反应放热,氢气的转化率减小,选项A错误;B、无论生成物是否是气体,增大压强反应速率和氢气的转化率都增大,选项B正确;C、充入氮气使体系压强增大,但是各种反应物的浓度并没有变化,碰撞几率依旧不变,所以平衡不移动,选项C错误;D、甲醇为液体时,分离出甲醇,对反应速率几乎无影响,选项D错误。答案选B。
,解得x=0.75,生成甲醇物质的量为0.75mol;④A、升高温度,氢气的反应速率增大,但该反应放热,氢气的转化率减小,选项A错误;B、无论生成物是否是气体,增大压强反应速率和氢气的转化率都增大,选项B正确;C、充入氮气使体系压强增大,但是各种反应物的浓度并没有变化,碰撞几率依旧不变,所以平衡不移动,选项C错误;D、甲醇为液体时,分离出甲醇,对反应速率几乎无影响,选项D错误。答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题: 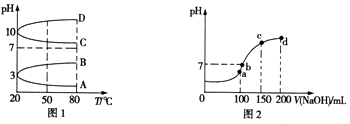
(1)相同条件下,相等浓度的NH4Al(SO4)2溶液中c(NH4+)NH4HSO4溶液中c(NH4+) (填“=”、“>”或“<”).
(2)如图1是0.1molL﹣1电解质溶液的pH随温度变化的图象. ①其中符合0.1molL﹣1 NH4Al(SO4)2的pH随温度变化的曲线是(填写字母).
②室温时,0.1molL﹣1 NH4Al(SO4)2溶液中2c(SO42﹣)﹣c(NH4+)﹣3c(Al3+)=molL﹣1(填
计算式).
(3)室温时,向100mL 0.1molL﹣1 NH4HSO4溶液中滴加0.1molL﹣1NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图2所示.图中a、b、c、d四个点,水的电离程度最大的是;在b点,溶液中各离子浓度由大到小的顺序是 .
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解质溶液为Na2CO3溶液,电解总反应的方程式为 .
(5)一种可超快充电的新型铝电池,充放电时AlCl4﹣和Al2Cl7﹣两种离子在Al电极上相互转化,其他离子不参与电极反应,放电时负极Al的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.被誉为改变未来世界的十大新科技之一的燃料电池。 右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.

试回答下列问题:
(1)燃料电池的优点是________;电解质溶液中的OH-移向______极(填“负”或“正”).
(2)写出氢氧燃料电池工作时正极反应式:_______________________。
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___________.
(4)利用该装置可以处理氮的氧化物和NH3 尾气,总反应为:6NO2 +8NH3=7N2+12H2O,负极反应式为__________。
II.将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:
(1)产生氢气的体积(标准状况)为________________;
(2)通过导线的电子数为__________(用NA表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是几种常见的化学电源示意图,有关说法不正确的是( ) 
A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池在长时间使用后,锌筒被破坏
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.铅蓄电池工作过程中,每通过 2 mol 电子,负极质量减轻 207 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃下,稀释HA、HB 两种酸溶液,溶液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积,a点时,HB溶液中B的物质的量分数 ,下列说法正确的是
,下列说法正确的是

A. HA、HB都是弱酸
B. 加水稀释过程中,δ(B )减小
C. NaB溶液中,c(Na+)=c(B-)+c(OH-)
D. 曲线上b、c两点c(B-)/[c(HB)·c(OH-)]相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,a、b、c、d、e 为元素周期表中前四周期的一部分元素,下列有关叙述正确的是( )

A. 元素 b 位于ⅥA 族,有+6、-2 两种常见化合价
B. 五种元素中,元素 e 的性质最稳定
C. 原子半径有 d>c>b
D. 元素 e 参与形成的化合物可以作为一种半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
有机化合物G是一种生物降解塑料,其合成路线如下:

己知:①![]() (R1、R2表示烃基)
(R1、R2表示烃基)
②E不能与银氨溶液发生反应,但能与Na反应。
③
(1)A的化学名称为________
(2)生成B的反应类型为________,生成C的反应类型为________
(3)由B生成C的化学方程式为________
(4)G的结构简式为________
(5)E的同分异构体很多,能同时满足下列条件的链状化合物共有________种(不含立体异构),其中核磁共振氢谱有4组峰值,且峰面积比为2:2:1:1的结构简式为_______。
①含有三种官能团;②能与新制的Cu(OH)2悬独液反应;③氧原子不与碳碳双键相连④与Na反应可放出氢气。
(6)写出用苯和CH3COCl为原料制备化合物![]() 的合成路线(无机试剂任选):_____。
的合成路线(无机试剂任选):_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示,下列说法正确的是

A. HS-在硫氧化菌作用下转化为SO42-的反应为:HS-+4H2O-8e-== SO42-+9H+
B. 电子从b流出,经外电路流向a
C. 如果将反应物直接燃烧,能量的利用率不会变化
D. 若该电池电路中有0.4mol电子发生转移,则有0.5molH+通过质子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害.在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)COS(g)+H2(g) K=0.1,反应前CO物质的量为10mol,平衡后CO为8mol.下列说法正确的是( )
A.保持其他条件不变,升高温度,H2S浓度增加,表明该反应是吸热反应
B.通入CO后,正反应速率逐渐增大
C.反应前H2S物质的量为7 mol
D.CO的平衡转化率为80%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com